
【题目】研究碳、氮及其化合物的转化对于环境的改善有重大意义。
(1)氧化还原法消除NOx的转化如下:NO![]() NO2
NO2![]() N2
N2
已知:NO(g)+O3(g)=NO2(g)+O2(g) ΔH=-200.9 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH=-116.2 kJ·mol-1
则反应Ⅰ的热化学方程式为_____________________________________________。
(2)有人设想将CO按下列反应除去:2CO(g)=2C(s)+O2(g) ΔH>0,请你分析该设想能否实现并说明理由是____________________________________________。
(3)甲酸的电离平衡常数Ka=1.70×10-4。向20 mL 0.1 mol·L-1的甲酸钠溶液中滴加10 mL 0.1 mol·L-1的盐酸,混合液呈________(填“酸”或“碱”)性,溶液中离子浓度从大到小的顺序为______________________。
(4)活性炭也可用于处理汽车尾气中的NO。在2 L恒容密闭容器中加入0.100 0 mol NO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量如表所示:
温度 | 固体活性炭/mol | NO/mol | A/mol | B/mol |
200 ℃ | 2.000 | 0.040 0 | 0.030 0 | 0.030 0 |
335 ℃ | 2.005 | 0.050 0 | 0.025 0 | 0.025 0 |
①该反应的正反应为________(填“吸热”或“放热”)反应。
②200 ℃时,平衡后向恒容容器中再充入0.1 mol NO,再次平衡后,NO的百分含量将________(填“增大”“减小”或“不变”)。
③计算反应在335 ℃时的平衡常数为________。
(5)工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5~26.5℃后用氨水吸收过量的CO2,该反应的化学方程式为_______________________。在用氨水吸收前,烟气需冷却至15.5~26.5℃的可能原因是____________________________。
【答案】3NO(g)+O3(g)=3NO2(g) ΔH=-317.1 kJ·mol-1 不能,该反应是焓增、熵减的反应,根据ΔG=ΔH-T·ΔS,ΔG>0 酸 c(Na+)>c(HCOO-)>c(Cl-)>c(H+)>c(OH-) 放热 不变 0.25 NH3·H2O +CO2= NH4HCO3 降低吸收过程中氨水的挥发,促进氨水对CO2的吸收
【解析】
(1)①NO(g)+O3(g)=NO2(g)+O2(g)△H=-200.9kJ/mol,②2NO(g)+O2(g)=2NO2(g)△H=-116.2kJ/mol,反应I的反应方程式为3NO+O3=3NO2,因此①+②得出3NO(g)+O3(g)=3NO2(g) △H=(-200.9kJ·mol-1-116.2kJ·mol-1)=-317.1kJ·mol-1;
(2)根据△G=△H-T△S,能够自发进行,说明△G<0;根据信息,该反应△H>0,该反应为熵减过程,即△S<0,复合判据△G>0,该反应不能自发进行;
(3)两种溶液混合后,溶质为HCOOH、HCOONa和NaCl,且三者物质的量相等,甲酸的电离平衡常数Ka=1.70×10-4,则HCOO-的水解平衡常数Kh=Kw/Ka=1×10-14/(1.7×10-4)=1/1.7×10-10<1.70×10-4,甲酸的电离程度大于HCOO-水解程度,溶液显酸性,离子浓度大小顺序是c(Na+)>c(HCOO-)>c(Cl-)>c(H+)>c(OH-);
(4)①根据表中数据,335℃平衡时NO的物质的量比200℃时大,说明升高温度,平衡向逆反应方向移动,即正反应为放热反应;
②根据表中200℃时各物质起始物质的量和平衡时物质的量可知,NO、固体活性炭、A、B转化物质的量依次为0.06mol、0.03mol、0.03mol、0.03mol,则NO、固体活性炭、A、B的化学计量数之比为2:1:1:1,该反应方程式为2NO(g)+C(s)![]() A(g)+B(g),活性炭为固体,再通入NO,相当于在原来的基础上增大压强,增大压强平衡不移动,NO的百分含量不变;
A(g)+B(g),活性炭为固体,再通入NO,相当于在原来的基础上增大压强,增大压强平衡不移动,NO的百分含量不变;
③335℃时K=![]() =
=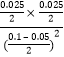 =0.25;
=0.25;
(5)氨水吸收过量的CO2,其反应的化学方程式为NH3·H2O+CO2=NH4HCO3;氨水易挥发,NH3·H2O受热易分解,因此冷却至15.5~26.5℃可能原因是降低吸收过程中氨水的挥发,促进氨水对CO2的吸收。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 将纯水加热至较高温度,Kw变大、pH变小、呈酸性
B. 常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C. 向0.1 mol·L-1醋酸溶液中加入少量冰醋酸,溶液的pH减小,醋酸电离程度变大
D. 等体积、pH都为3的酸HA和HB分别与足量的Zn反应,HA放出的H2多,说明HA的酸性小于HB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只可能含有下列离子中的几种:K+、NO![]() 、SO
、SO![]() 、NH
、NH![]() 、CO
、CO![]() (不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
(不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;(已知NH4+在碱性条件下可以生产氨气)
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g。
下列说法正确的是( )
A. 该溶液中无法确定是否含有K+
B. 该溶液中肯定含有NO![]() 、SO
、SO![]() 、NH
、NH![]() 、CO
、CO![]()
C. 不能确定该溶液中是否含有NO![]()
D. 该溶液中一定含K+,且c(K+)= 0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知pOH=-lgc(OH-)。T℃时,往50mL0.1mol·L-1MOH溶液中滴加0.1mol·L-1盐酸,溶液pH、pOH随滴入盐酸体积的变化如下图所示,以下说法正确的是
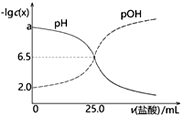
A. 盐酸与MOH溶液恰好中和时溶液pH=6.5
B. a=12
C. 盐酸滴定MOH实验中选择酚酞做指示剂比选甲基橙误差更小
D. T℃时,MOH的电离平衡常数Kb约为1.0×10-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】定量分析是化学实验中重要的组成部分。
Ⅰ.中和热的测定:在实验室中,用50 mL 0.40 mol/L的盐酸与50 mL 0.50mol/L的NaOH溶液反应测定中和热。假设此时溶液密度均为1 g/cm3,生成溶液的比容热c = 4.18 J/(g℃),实验起始温度为T1℃,终止温度为T2℃,则中和热△H=___kJ/mol。
Ⅱ.氧化还原滴定实验与中和滴定类似。为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L KMnO4标准溶液滴定。
(1)滴定原理为:(用离子方程式表示)___________。
(2)达到滴定终点时的颜色变化为___________ 。
(3)如图表示50mL滴定管中液面的位置,此时滴定管中液面的___________读数为mL。

(4)为了减小实验误差,该同学一共进行了三次实验,假设每次所取H2C2O4溶液体积均为VmL,三次实验结果记录如下:
实验序号 | ① | ② | ③ |
消耗KMnO4溶液体积/mL | 26.53 | 24.02 | 23.98 |
从上表可以看出,实验①中记录消耗KMnO4溶液的体积明显多于②③,其原因可能是 ______________________。
A.滴加KMnO4溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
B.①滴定盛装标准液的滴定管装液前用蒸馏水清洗过,未用标准液润洗,②③均用标准液润洗
C.实验结束时俯视刻度线读取滴定终点时KMnO4溶液的体积
D.①滴定用的锥形瓶用待测液润洗过,②③未润洗
(5)H2C2O4的物质的量浓度=______________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X和Y形成能够离子化合物XY2。且该离子化合物中阴、阳离子具有相同的电子层结构。下列说法不正确的是( )
A.离子半径:X2+<Y-
B.原子序数:X<Y
C.该化合物中只存在离子键
D.原子最外层电子数X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理解释的是
A. 工业制硫酸采用二氧化硫催化氧化,高温可以提高单位时间SO3的产量
B. 合成氨工业中使用铁触媒做催化剂
C. 用饱和食盐水除去氯气中氯化氢杂质
D. 容器中有2HI(g)![]() H2(g)+I2(g),增大压强颜色变深
H2(g)+I2(g),增大压强颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AG均分别代表一种物质,结合如图所示的转化关系(框图中的部分产物已略去),回答下列问题:

已知:I.天然有机高分子化合物A,是一种遇到碘水能变蓝的多糖;
Ⅱ. H为丙三醇(CH2OH-CHOH-CH2OH),G有香味。
(1)①C→E的反应类型为_________。
②与出D→C的化学反应方程式:_________。
③写出F与H以物质的量3:1浓硫酸、加热条件下发生的化学方程式:_____。
(2)人在剧列运动后腿和胳膊会感到酸胀或疼痛,原因之一是B(C6H12O6)→2C3H6O3(乳酸)。某研究小组为了研究乳酸(无色液体,与水混溶)的性质,做了如下实验:
①取90g乳酸饱和NaHCO3溶液反应,测得生成的气体体积为22.4L(标准状况下);
②另取90g乳酚与过量的金属钠反应,测得生成的气体体积为22.4L(标准状况下)。
由以上实验推知乳酸分子含有的官能团名称________;试写出所有符合上述条件有机物的同分异构体的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒及其化合物在生产、生活中有着广泛的应用,掺杂硒的纳米氧化亚铜常用作光敏材料、电解锰行业催化剂等。
(1)酸性溶液中Na2SO3将H2SeO3和H2SeO4还原为晒单质的反应如下:
H2SeO3(aq)+2SO2(g)+H2O(l)=Se(s)+2H2SO4(aq) △H1
2H2SeO4(aq)+Se(s)+H2O(l)=3H2SO4(aq) △H2
H2SeO4(aq)+2SO2(g)+2H2O(l)=Se(s)+3H2SO4(aq) △H3
实验中控制其他条件不变(盐酸浓度等),![]() 与硒还原率关系如图1。在A点之前,随着
与硒还原率关系如图1。在A点之前,随着![]() 的增加,Se的还原率不断升高的原因是_____________。
的增加,Se的还原率不断升高的原因是_____________。
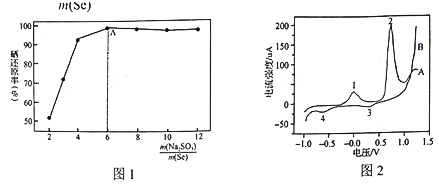
(2)向Na2SeO3溶液中加入适量的AgNO3溶液,得到Ag2Se纳米晶体,同时产生N2。该反应的离子方程式为 ______。
(3)制 PbSe 纳米管时还产生了副产物PbSeO3。己知:Ksp(PbSeO3)=3×l0-12, Ksp(PbSe)= 3×l0-38。为了除去PbSe中混有的PbSeO3,可以采取的措施是______。
(4)实验室测得碱性条件下PbSe纳米管在电极表面的氧化还原行为,结果如图2所示。其中一条曲线上的峰表示氧化过程,另一条曲线上的峰表示还原过程。整个过程共发生如下变化:Pb(OH)2—PbO2;Pb(OH)2—Pb; PbSe—Se; PbO2→Pb(OH)2,各物质均难溶于水。峰1对应的电极反应式为:PbSe-2e-+2OH-=Pb(OH)2+Se;则峰2对应的电极反应式为 ______。
(5)掺杂硒的纳米Cu2O催化剂可用于工业上合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) △H=akJ/mol。按n(H2):n(CO)=1:1的投料比将H2与CO充入VL的恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如下图所示。
CH3OH(g) △H=akJ/mol。按n(H2):n(CO)=1:1的投料比将H2与CO充入VL的恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如下图所示。
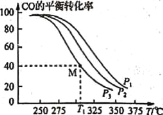
①压强P1、P2、P3由小到大的顺序是 __________。
②T1 ℃时若向该容器中充入2.0 mol H2和2.0 mol CO发生上述反应,5 min后反应达到平衡(M点),则M点对应条件下反应的平衡常数为 ______。
(6)将CuCl水解再热分解可得到纳米Cu2O。CuCl 水解的反应为 CuCl(s) +H2O(1) ![]() CuOH(s)+Cl-(aq)+H+(aq),该反应的平衡常数 K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为K=________。
CuOH(s)+Cl-(aq)+H+(aq),该反应的平衡常数 K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为K=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com