
A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去)。
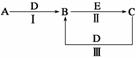
(1)若A是能使湿润红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体。
①C的电子式为______________。
②写出反应Ⅰ的化学方程式_______________________________________________。
③写出反应Ⅱ的化学方程式_______________________________________ ________。
________。
(2)若A是淡黄色化合物;常温下D是无色气体;C中含有的阴、阳离子均为10电子粒子。
①D的结构式为_________ ___,C中所含化学键的类型是____________________。
___,C中所含化学键的类型是____________________。
②写出反应Ⅰ的化学方程式_______________________________________________。
③写出反应Ⅱ的化学方程式_______________________________________________。
 (3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。
(3)将(2)中一定量的气体D通入2 L C的溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。
①O点溶液中所含溶质的化学式为__________,常温下a点溶液的pH________(填“>”、“=”或“<”)7,a点溶液中各离子浓度由大到小的关系是_____________________
________________________________________________________________________。
②标况下,通入气体D的体积为__ ________L,C溶液的物质的量浓度为________
________L,C溶液的物质的量浓度为________
mol·L-1。
答案 (1)① N⋮⋮N
N⋮⋮N
②4NH3+5O2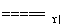 4NO+6H2O
4NO+6H2O
③2NO+2CO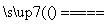 N2+2CO2
N2+2CO2
(2)①O===C===O (极性)共价键、离子键
②2Na2O2+2CO2===2Na2CO3+O2
③Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
(3)①NaOH、Na2CO3 > c(Na+)>c(Cl-)>c(HCO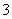 )>c(OH-)>c(H+)>c(CO
)>c(OH-)>c(H+)>c(CO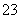 )
)
②44.8 2.5
解析 (1)A是能使湿润红色石蕊试纸变蓝的气体,说明其为NH3,C、D为空气的主要成分,且D能与A反应,故D为O2,C为N2。反应 Ⅰ 为氨的催化氧化反应,那么B为NO,NO与有毒气体E反应可生成N2,说明E具有还原性,故其为CO。
(2)A是淡黄色化合物,故A是Na2O2,常温下D是无色气体且能与Na2O2反应,故D必为CO2。Na2O2与CO2反应生成B,那么B为Na2CO3,Na2CO3经反应Ⅱ可得到C,C中的阴、阳离子都含10个电子,故其为NaOH。
(3)分析图像可知,加入盐酸时,开始没有气体产生,加到一定的量时,才产生气体。故溶液中的溶质为NaOH、Na2CO3,在a点开始产生气体,说明a点的溶质为NaHCO3和NaCl,故其溶液呈碱性,其离子浓度大小关系为c(Na+)>c(Cl-)>c(HCO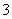 )>c(OH-)>
)>c(OH-)>
c(H+)>c(CO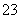 )。从a点开始是NaHCO3与盐酸反应,消耗盐酸的物质的量为2 mol,故NaHCO3的物质的量为2 mol,由碳元素守恒可得,n(NaHCO3)=n(CO2)=2 mol,故标况
)。从a点开始是NaHCO3与盐酸反应,消耗盐酸的物质的量为2 mol,故NaHCO3的物质的量为2 mol,由碳元素守恒可得,n(NaHCO3)=n(CO2)=2 mol,故标况 下CO2的体积为44.8 L。NaHCO3恰好反应完时消耗的盐酸的物质的量为5 mol,此时溶液中的溶质全部为NaCl,由氯和钠元素守恒可得:n(HCl)=n(NaCl)=n(NaOH)=5 mol,故c(NaOH)=
下CO2的体积为44.8 L。NaHCO3恰好反应完时消耗的盐酸的物质的量为5 mol,此时溶液中的溶质全部为NaCl,由氯和钠元素守恒可得:n(HCl)=n(NaCl)=n(NaOH)=5 mol,故c(NaOH)=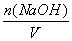 =
=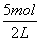 =2.5 mol·L-1。
=2.5 mol·L-1。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
大气平流层中O2吸收紫外线可变成臭氧(O3),而冰箱中的制冷剂氟里昂在紫外线作用下分解出氯原子,氯原子能加速臭氧的分解,从而破坏平流层中的臭氧层。同样超音速飞机的尾气及发动机尾气中的NO也能加快O3的 分解,反应式如下:NO+O3===NO2+2O;NO2+O===NO+O2。请你写出总的反应式: ______________;其中NO的作用是______________和____________。
分解,反应式如下:NO+O3===NO2+2O;NO2+O===NO+O2。请你写出总的反应式: ______________;其中NO的作用是______________和____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的沸点由高到低排列的顺序是( )
① CH3(CH2)2CH3 ② CH3(CH2)3CH3 ③ (CH3)3CH ④ (CH3)2CHCH2CH3 ⑤ (CH3CH2)2CHCl
A.⑤②④①③ B.④②⑤①③ C.⑤④②①③ D.②④⑤③①
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的化学方程式,并注明反应类型。(有机物用结构简式表示)
(1)由异戊二烯制备聚异戊二烯
反应类型:
(2)用甲苯制TNT 反应类型:
(3)实验室制取乙烯 反应类型:
(4)丙烯与溴化氢反应 反应类型:
查看答案和解析>>
科目:高中化学 来源: 题型:
已知有以下物质相互转化。
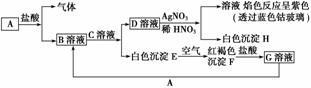
试回答下列问题:
(1)B的化学式为______________________,D的化学式为______________________。
(2)由E转变成F的化学方程式为___________________________________________。
(3)用KSCN鉴别G溶液的离子方程式为____________________________________;
向G溶液加入A的有关离子反应方程式为____________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D四种短周期元素,它们之间的关系如下。原子半径:A<C<B<D;原子的最外层电子数:A+C=B+D=8;原子的核外电子层数:B=C=2A;B元素的主要化合价:最高正价+最低负价=2。下列有关说法错误的是( )
A.由A、B两种元素组成的一种常见气体显碱性
B.D元素组成的单质能与强碱溶液反应,并有H2生成
C.C元素不可能在第1周期,也不可能在第ⅣA族
D.A、B、C、D四种元素组成的离子化合物中一定含有金属阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素,原子序数依次增大。A、D同族,B、C同周期。A、B组成的化合物甲为气态,其中A、B的原子数之比为4∶1,由A、C组成的两种化合物乙、丙都是液态,乙中A、C原 子数之比为1∶1,丙中A、C原子数之比为2∶1,由D、C组成的两种化合物丁和戊都是固体,丁中D、C原子数之比为1∶1,戊中D、C原子数之比为2∶1,写出下列物质的化学式:甲____________,乙____________,丙____________,丁____________,戊____________。
子数之比为1∶1,丙中A、C原子数之比为2∶1,由D、C组成的两种化合物丁和戊都是固体,丁中D、C原子数之比为1∶1,戊中D、C原子数之比为2∶1,写出下列物质的化学式:甲____________,乙____________,丙____________,丁____________,戊____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在指定的条件下,下列各组离子能大量共存的是( )
A.使甲基橙变红的溶液中:Fe2+、Na+、I-、NH4+
B.强碱性溶液中:K+、Na+、ClO-、S2-
C.0.1 mol·L-1 NaAlO2溶液中:H+、Na+、Cl-、SO42-
D.由H2O电离出的c(H+)=10-11mol/L溶液中:Na+、HCO3-、AlO2-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com