
【题目】常温常压下,H2和O2在Ag9(图中物质1)团簇上生成H2O2的吉布斯自由能(![]() )的部分变化曲线如图。下列说法错误的是( )
)的部分变化曲线如图。下列说法错误的是( )
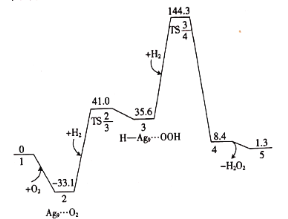
A.物质2中的O2是处于被吸附活化状态
B.物质3→物质4的过程中活化吉布斯自由能能垒为![]()
C.物质4可能为![]()
D.反应![]() 具有自发性
具有自发性
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】NH4HCO3的分解温度是 35℃。以氯化钾和制取二氧化钛的副产品硫酸亚铁为原料生产铁红颜料和过二硫酸铵等,原料的综合利用率较高。其主要流程如下:
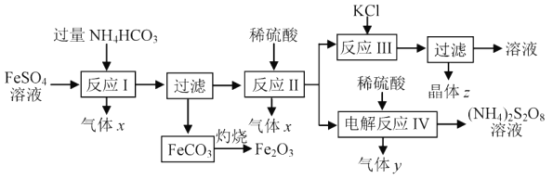
(1)气体x是_________,反应 I 需控制反应温度低于35℃ , 其目的是_______。
(2)反应I的离子方程式为 ___________,FeCO3灼烧的反应方程式为 __________。
(3)各物质的溶解度曲线如图,晶体z是____,简述反应III发生的原因 ________,工业生产上常在反应III的过程中加入一定量的乙醇,其目的是_____________。
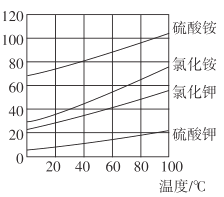
(4)反应IV 常用于生产(NH4)2S2O8 (过二硫酸铵)。电解时均用惰性电极,气体y是__________,阳极发生的电极反应可表示为_______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 在医药合成中有着广泛的用途。下列有关该物质的说法正确的( )
在医药合成中有着广泛的用途。下列有关该物质的说法正确的( )
A.该化合物中含氧官能团为酯基
B.该化合物中的所有碳原子一定处于同一平面内
C.该化合物可发生取代反应、加成反应和氧化反应
D.该化合物的同分异构体中,苯环上有两个取代基的共3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是一种重要的化工产品。
(1)标准状况下,1 mol NH3的体积约为________L。
(2)实验室制取NH3的化学方程式为______________。
(3)收集NH3应使用________法,要得到干燥的NH3可选用___做干燥剂。
(4)压强对合成氨反应具有重要的影响。下表是反应达到平衡时压强与 NH3 含量的一些实验数据:
压强MPa | 10 | 20 | 30 | 60 | 100 |
NH3含量(体积分数%) | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
从表中数据可以推断:随着压强增大,平衡时NH3含量随之___(填字母)。
A.增大 B.减小 C.先增大再减小 D.不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各溶液中,离子一定能大量共存的是( )
A.使甲基橙试液变红的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
B.常温下,![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
C.溶质为![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
D.水电离出的![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用冶铅废渣(含Pb、PbO、PbS及Zn、Fe、Cu等杂质)制取立德粉和回收铅的工艺流程如下:
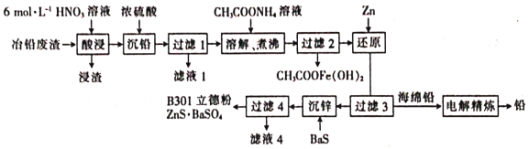
(1)“酸浸”时,PbS被氧化生成S,硝酸被还原为NO,则氧化0.3 mol PbS时,消耗HNO3______mol。
(2)“溶解、煮沸”时会发生多个反应。
①PbSO4溶解的离子方程式为__________________。(已知:Pb(CH3COO)2是弱电解质)
②“沉铅”时生成的沉淀中混有Fe3+,煮沸时醋酸铁水解的化学方程式为__________________。
(3)海绵铅(含少量Zn、Cu等杂质)进行“电解精炼”时,用PbSiF6、H2SiF6的混合溶液作电解液,海绵铅作_____(填“阳”或“阴”)极,阳极泥的主要成分是______(填化学式)。
(4)B301立德粉(ZnS·BaSO4)中ZnS的理论含量为29.4%。
①若要生产ZnS的理论含量为62.5%的B311高ZnS立德粉,可用的原料除BaS外,另两种原料可能为______。(填标号)
A. ZnSO4 B.NaCl C. ZnCl2 D. Na2SO4
②测定立德粉中ZnS的含量常用酸溶,调节pH至1~3,然后滴定形成K2Zn3[Fe(CN)6]2沉淀,该沉淀的溶度积常数Ksp的表达式为______。
(5)滤液4经加热后可返回______工序循环使用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式:
(1)丙烯制备聚丙烯:______;
(2)2-甲基-1,3-丁二烯与Br2的1,4-加成反应______;
(3)1,2-二溴乙烷在氢氧化钠、乙醇中加热______;
(4)实验室制备乙炔气体:______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Calanolide A是一种抗HIV药物,其结构简式如下图所示。已知:碳原子上连有4个不同的原子或基团时,该碳称为手性碳。下列关于Calanolide A的说法不正确的是( )
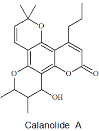
A.分子中有3个手性碳原子
B.分子中有5种含氧官能团
C.能发生消去反应、加成反应、氧化反应和还原反应
D.1molCalanolide A最多消耗2molNaOH或5molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组为探究![]() 的性质,将
的性质,将![]() 固体隔绝空气加热进行实验。已知加热会生成硫酸钠和另一种中学常见物质,加热前后,固体的质量没有变化。取加热后的固体溶于水,滴加稀盐酸,出现淡黄色沉淀。
固体隔绝空气加热进行实验。已知加热会生成硫酸钠和另一种中学常见物质,加热前后,固体的质量没有变化。取加热后的固体溶于水,滴加稀盐酸,出现淡黄色沉淀。
(1)生成的淡黄色沉淀是________(填名称)。
(2)写出![]() 固体隔绝空气加热的化学方程式_________。
固体隔绝空气加热的化学方程式_________。
(3)设计实验证明分解后产物中的硫酸钠固体__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com