
| A. | 2Al2O3(熔融) $\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑ | |
| B. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| C. | Fe+CuSO4═FeSO4+Cu | |
| D. | 2NaCl(水溶液)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ |
分析 金属冶炼是工业上将金属从含有金属元素的矿石中还原出来的生产过程.金属的活动性不同,可以采用不同的冶炼方法.
金属冶炼的方法主要有:
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
合电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al).
解答 解:A、铝很活泼,加入冰晶石降低氧化铝的熔点,工业上电解熔融氧化铝冶炼铝,故A正确;
B、铁位于金属活动顺序表中间位置的金属,通常用热还原法冶炼,故B正确;
C、铁比铜活泼,能从铜的盐溶液中置换出铜,故C正确;
D.氢离子的氧化性比钠离子强,在溶液中电解,氢离子放电,钠离子不放电,电解NaCl水溶液得不到金属钠,故D错误.
故选D.
点评 本题考查了金属冶炼的一般原理,难度不大,注意根据金属的活泼性不同采取相应的冶炼方法.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②④ | C. | ②③⑤ | D. | 只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑦ | B. | ①③④ | C. | ②④⑥ | D. | ④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 混合溶液的pH等于7 | B. | 混合溶液的pH大于7 | ||
| C. | 加入酸碱的物质的量相等 | D. | 混合溶液还能再中和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( )
将镁片、铝片平行插入到一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述正确的是( )| A. | 镁比铝活泼,镁失去电子被氧化成Mg2+ | |
| B. | 铝是电池负极,开始工作时溶液中会立即有白色沉淀生成 | |
| C. | 该装置的内、外电路中,均是电子的定向移动形成电流 | |
| D. | 该装置开始工作时,铝片表面的氧化膜可不必处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在一个基态多电子的原子中,不可能有两个能量完全相同的电子 | |
| B. | 金属Na、Mg、Al的硬度依次降低 | |
| C. | 由原子间通过共价键而形成的晶体一般具有高的熔、沸点及硬度 | |
| D. | PCl3和CO32-的中心原子的杂化方式相同,都是sp3杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E为周期表中原子序数依次递增的前四周期元素.
A、B、C、D、E为周期表中原子序数依次递增的前四周期元素.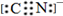 ,
,
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤,可以除去NaCl溶液中少量的淀粉胶体 | |
| B. | 溶解、过滤,可以提纯含少量BaSO4的BaCO3 | |
| C. | 加热蒸发,可以除去粗盐中的CaCl2、MgCl2等杂质 | |
| D. | 加入足量铁屑,充分反应后,过滤,可以除去FeCl2溶液中少量FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将气体通入高锰酸钾酸性溶液和溴水,溶液颜色无变化,该气体一定是甲烷 | |
| B. | 在导管口点燃该气体,火焰呈淡蓝色,用内壁涂有澄清石灰水的烧杯罩在火焰上方,烧杯壁上有白色物质产生,该气体一定是甲烷 | |
| C. | 在导管口点燃该气体,火焰呈淡蓝色,用干燥的冷烧杯罩在火焰上方,烧杯壁上有水珠产生,该气体一定是甲烷 | |
| D. | 若上述B和C的现象均能出现,则可判断该气体一定是甲烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com