
�ش��������⣺
(1)��Ͳ��Һ���������ȷ����Ϊ10.0 mLʱ��ȫ�������ձ��ڵ�ʵ�����________(����ڡ�����С�ڡ����ڡ�����ͬ)10.0 mL����100 mL����ƿ�ڵ���Һȷ���ݺ�ȫ�������Լ�ƿ���Լ�ƿ����Һ��ʵ�����________100 mL��
(2)��������ѧ��ѧʵ���г����ļ��ֶ���������
a����Ͳ
b������ƿ
c���¶ȼ�
d��������ƽ
�����б�ʾ������ʹ���¶ȵ���________(��д��ţ���ͬ)��
��ʹ��ǰҪ��������Ƿ�©Һ����________��
�۳�ȡ10.5 g������Ʒ(1 g����ʹ������)ʱ��������Ʒ������ƽ�����̣���������Ʒ��ʵ������Ϊ________g��
�����𰸣�
(1)���ڡ�С������
(2)��ab����b����9.5������ʾ��
(1)��ѧ������Ͳ�����ʾ�Ŀ̶�ֵ���ڵ���Һ������������ƿ�Ŀ̶�ֵ�Ƕ���ʱ�����ݻ�������ʱ����ƿ����Ҫ����һЩҺ�壬�ʵ�����Һ�����С������ƿ��ʾ�����������
(2)��Ͳ������ƿ��������������Һ��������Һ��������¶ȵ�Ӱ�죬��˶���Ҫ�����¶ȣ�����ƿʹ��ǰ��Ҫ�����Ƿ�©Һ��m(����)��m(����)��m(����)����Ŀ�������������10 g��������0.5 g����m(��)��0.5��10 g��m(��)��9.5 g��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶�/�� | 400 | 500 | 830 | 1000 |
| ƽ�ⳣ��K | 10 | 9 | 1 | 0.6 |
| [H2]?[CO2] |
| [CO]?[H2O] |
| [H2]?[CO2] |
| [CO]?[H2O] |
| A | B | C | D | |
| n��CO2�� | 3 | 1 | 0 | 1 |
| n��H2�� | 2 | 1 | 0 | 1 |
| n��CO�� | 1 | 2 | 3 | 0.5 |
| n��H2O�� | 5 | 2 | 3 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�




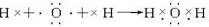
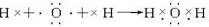






�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
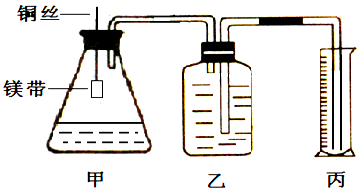
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com