
【题目】(1)在101kPa时,H2在1mol O2中完全燃烧生成2mol液态水,放出571.6kJ的热量,H2的燃烧热为___,表示H2燃烧热的热化学方程式为___。
(2)①已知:CH4(g)+H2O(g)=CO(g)+3H2(g) △H= +206.2kJ·mol-1,CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247.4kJ·mol-1,则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:____。
②由气态基态原子形成1mol化学键释放的最低能量叫键能。已知表中所列键能数据,则N2(g)+3H2(g)![]() 2NH3(g) △H=__kJ·mol-1。
2NH3(g) △H=__kJ·mol-1。
化学键 | H-H | N-H | N≡N |
键能kJ·mol-1 | 436 | 391 | 945 |
【答案】285.8kJ/mol H2(g)+![]() O2(g)=H2O(l) △H= -285.8kJ·mol-1 CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H= +165.0kJ·mol-1 -93
O2(g)=H2O(l) △H= -285.8kJ·mol-1 CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H= +165.0kJ·mol-1 -93
【解析】
(1)在101kPa时,1mol H2(g)完全燃烧生成稳定的氧化物时,释放的热量为燃烧热;
(2)①根据盖斯定律求解;
(1)在101kPa时,反应物为2mol H2(g)、1mol O2(g),H2O(l)为生成物,燃烧热为1mol H2(g)完全燃烧生成液态水时释放的热量,则燃烧热为285.8kJ/mol;燃烧热的热化学方程式为H2(g)+![]() O2(g)═H2O(l) △H= -285.8kJ·mol-1;
O2(g)═H2O(l) △H= -285.8kJ·mol-1;
(2)① i CH4(g)+H2O(g)═CO(g)+3H2(g) △H= +206.2kJ·mol-1,ii CH4(g)+CO2(g)═2CO(g)+2H2(g) △H= +247.4kJ·mol-1,根据盖斯定律,i×2-ii即可得到CH4(g)+2H2O(g)═CO2(g)+4H2(g),则△H= +206.2kJ/mol×2-247.4kJ/mol= +165.0kJ·mol-1;
②化学反应中,旧键的断裂吸收热量,新键的形成释放热量,则△H=945+436×3-391×6= -93kJ·mol-1。


科目:高中化学 来源: 题型:
【题目】在0.2 L由NaCl溶液、MgCl2溶液、CuCl2溶液组成的混合溶液中,部分离子的浓度如图所示。
(1)混合液中,NaCl的物质的量为_______mol,MgCl2的质量为_______g。
(2)该混合溶液中CuCl2的物质的量浓度为_____molL﹣1,将该混合溶液加水稀释至体积为1 L,稀释后溶液中Cu2+的物质的量浓度为_______molL﹣1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘氨酸亚铁络合物[(H2NCH2COO)2Fe]是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法,如图:
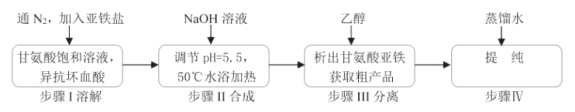
已知:

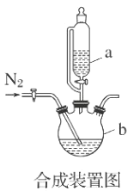
请回答:
(1)合成装置中仪器a中玻璃导管的作用是__。
(2)合成过程中,本实验为了防止Fe2+被氧化,采取的措施有__,__。
(3)写出水浴加热过程中生成甘氨酸亚铁络合物的离子方程式___。
(4)下列说法正确的是__。
A.滴入液体前,应先打开滴液漏斗a的上口玻璃塞
B.根据题中所给信息,亚铁盐应选用FeSO4·7H2O
C.步骤Ⅲ中的分离方法是过滤
D.步骤IV,提纯操作中的干燥过程最好选用真空干燥
(5)合成过程需控制pH=5.5,试说明理由___。
(6)步骤Ⅲ加入无水乙醇的目的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2mol钠和1mol铝的混合物小心地投入932g水中,充分反应,计算:
(1)生成气体的质量为多少______?
(2)溶液中有几种溶质______?
(3)各溶质的质量分数为多少______?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:3A(气)![]() 3B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是 ( )
3B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是 ( )
A. B和C可能都是固体B. B和C一定都是气体
C. 若C为气体,则B一定是固体D. B和C可能都是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu、Zn及其化合物在生产、生活中有着重要作用。请回答:
(1)Cu、Zn在周期表中________区,焰色反应时Cu的4s电子会跃迁至4p轨道,写出Cu的激发态电子排布式___________。
(2)分别向CuSO4、MgSO4溶液加氨水至过量,前者为深蓝色溶液,后者为白色沉淀。
①NH3与Cu2+形成配合物的能力大于Mg2+的原因为_________________。
②溶液中的水存在H3O+、![]() 等微粒形式,
等微粒形式,![]() 可看作是H3O+与H2O通过氢键形成的离子,则
可看作是H3O+与H2O通过氢键形成的离子,则![]() 的结构式为___________。
的结构式为___________。
(3)Zn的某种化合物M是很好的补锌剂,结构式如图:

①1 mol M含有的σ键的数目为___________。
②常见含氮的配体有 H2NCH2 COOˉ、NH3、![]() 等,NH3的分子空间构型为____________,
等,NH3的分子空间构型为____________,![]() 的中心氮原子杂化方式为__________。
的中心氮原子杂化方式为__________。
③M在人体内吸收率高的原因可能是锌形成配合物后,电荷__________(填“变多”“变少”或“不变”),可在消化道内维持良好的稳定性。
(4)卤化锌的熔点如表:
卤化锌/ ZnX2 | ZnF2 | ZnCl2 | ZnBr2 |
熔点/℃ | 872 | 283 | 394 |
则ZnX2熔点如表变化的原因是____________________。
(5)Zn的某种硫化物的晶胞如图所示。已知S2-和Zn2+的半径分别为r1 pm、r2 pm,且S2-与Zn2+相切,NA为阿伏加德罗常数的值。则该晶体的密度为________g·cm-3(写计算表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷和丙烷的混合气体完全燃烧后,先将产物通过浓硫酸,浓硫酸增重30.6 g ,然后通过碱石灰,碱石灰增重52.8 g,混合气体中乙烷和丙烷的体积比为( )
A.1∶1
B.2∶3
C.3∶2
D.3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】800℃时,在2 L密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2(g),该反应体系中n(NO)随时间的变化如下表:
2NO2(g),该反应体系中n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.022 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
下列有关说法不正确的是
A. 用氧气表示0~3 s内该反应的平均速率ν(O2)=0.0025 mol·L-1·s-1
B. 容器内颜色保持不变时,说明该反应达到平衡状态
C. 增大氧气的浓度,既加快反应速率,又使平衡正向移动
D. 该反应达到平衡时,转移电子总数为0.03NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学就在我们身边,它与我们的日常生活密切相关,按要求回答以下问题:
(1)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是_________________.
(2)硅酸盐常可写成氧化物形式,钾长石(K2Al2Si6O16)写成氧化物的形式为____________.
(3)漂粉精中有效成分的化学式为_________________.
(4)“硅材料”是无机非金属材料的主角,其中广泛应用的光导纤维成分是_____________________
(5)陶瓷、水泥和玻璃是常用的传统的无机非金属材料,其中生产普通玻璃的主要原料有_________,氢氧化钠溶液不能用玻璃塞的原因是(化学方程式)_________________.
(6)向浑浊的水中加入明矾KAl(SO4)212H2O后,水可得到净化.写出明矾在水中的电离方程式_______,往明矾溶液中逐滴加入Ba(OH)2溶液直至Al3+恰好沉淀完全,发生反应的离子方程式为_________________ .
(7)饮用水中的NO3-对人类健康产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.
请回答下列问题:
①在化学方程式上用单线桥标出该反应中电子转移的方向和数目:_________________.
②上述反应中若生成标况下3.36L N2,则转移的电子数目为:_________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com