
 某学习小组用下列实验方案来制备乙酸乙酯,装置(夹持装置省略)如图.
某学习小组用下列实验方案来制备乙酸乙酯,装置(夹持装置省略)如图.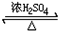 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.| 密度/(g•cm-3) | 沸点/℃ | |
| 乙酸 | 1.05 | 118.1 |
| 乙醇 | 0.780 | 78.3 |
| 乙酸乙酯 | 0.905 | 77.2 |
分析 (1)沸点低的液体加热,应加入碎瓷片,防止暴沸;
(2)生成乙酸乙酯为乙酸、乙醇间的酯化反应,本质为酸脱羟基,醇脱氢,相互结合生成水和乙酸乙酯;
(3)生成乙酸乙酯的蒸汽经冷凝进入锥形瓶,有气体存在的反应且有连接装置的仪器实验前要检验装置的气密性;冷凝管水流遵循逆流原理,这样冷凝效果好;乙酸乙酯 沸点77.2℃;
(4)乙酸乙酯不溶于碳酸钠溶液,可以通过分液操作分离;
(5)增大乙酸或乙醇的浓度或减小水或乙酸乙酯的浓度,能够提高酯的产率.
解答 解:(1)液体乙酸乙醇沸点低,加入沸石(碎瓷片),可以通过沸石(碎瓷片)孔隙凝聚蒸汽,使成为气泡浮出,防止暴沸,
故答案为:防止液体暴沸;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应方程式为:CH3CH2OH+CH3COOH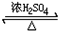 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
故答案为:CH3CH2OH+CH3COOH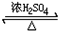 CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(3)生成乙酸乙酯的蒸汽经冷凝进入锥形瓶,该装置在实验前要检验装置的气密性,如果气密性较差,生成的乙酸乙酯气体逸出不仅污染大气,还导致实验失败,冷凝管水流方向应从下到上与蒸汽流动方向相反,即b进a出,乙酸乙酯 沸点77.2℃,温度最好控制在77.2℃,
故答案为:检查装置的气密性;b进a出;77.2;
(4)乙酸乙酯不溶于碳酸钠溶液,乙酸乙酯遇碳酸钠溶液,混合液会分层,可以通过分液操作分离出乙酸乙酯,
故答案为:分液;
(5)乙酸与乙醇在浓硫酸作用下加热发生酯化反应位可逆反应:CH3CH2OH+CH3COOH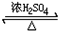 CH3COOCH2CH3+H2O,增大乙酸或乙醇的浓度或减小水或乙酸乙酯的浓度,能够提高酯的产率,使用浓硫酸吸水、把酯蒸出反应体系、提高醇的用量比例等,
CH3COOCH2CH3+H2O,增大乙酸或乙醇的浓度或减小水或乙酸乙酯的浓度,能够提高酯的产率,使用浓硫酸吸水、把酯蒸出反应体系、提高醇的用量比例等,
故答案为:使用浓硫酸吸水、把酯蒸出反应体系、提高醇的用量比例等(能回答出两条措施即可).
点评 本题考查了乙酸乙酯的制备,为高频考点,把握制备原理、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意有机物的性质,题目难度不大.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3 | |
| B. | 乙醇溶液和双氧水均可用于杀菌消毒,其原理相同 | |
| C. | 用玻璃棒蘸取酸性高锰酸钾溶液,滴在pH试纸上,然后与标准比色卡对照,测其pH | |
| D. | “一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”的简称,丝绸的主要成分是天然纤维素,属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂和蛋白质在一定条件下一定都能水解 | |
| B. | 除去乙醇中的乙酸用分液的方法 | |
| C. | C5H10O2能与NaHCO3反应的结构有4种 | |
| D. | C8H10的同分异构体有三种,它们的性质相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作和现象 | 结论 |
| A | 将Fe(NO3)2样品溶于稀H2SO4,溶液呈黄色. | Fe(NO3)2样品已被氧化变质 |
| B | 室温下,向 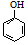 浊液中滴加Na2CO3溶液,浊液变澄清. 浊液中滴加Na2CO3溶液,浊液变澄清. | CO32-结合H+的能力比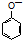 的强 的强 |
| C | 向Na2SiO3溶液中滴加稀硫酸,出现白色胶状沉淀. | 非金属性:S>Si |
| D | 向BaSO4中加入饱和Na2CO3溶液,充分搅拌,静置,过滤,洗涤.向滤渣中加盐酸,有气泡产生. | Ksp(BaCO3)<Ksp(BaSO4) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙二醇与丙三醇互为同系物 | B. | 乙烯和丙烯具有相似的化学性质 | ||
| C. | 淀粉和纤维素属于同分异构体 | D. | 乙酸与甲酸甲酯均易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
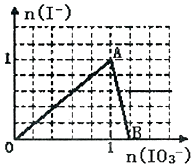 在含3molNaHSO3的溶液中加入含a mol NaIO3的溶液充分反应(不考虑I2+I-?I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如图所示,下列说法不正确的是( )
在含3molNaHSO3的溶液中加入含a mol NaIO3的溶液充分反应(不考虑I2+I-?I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如图所示,下列说法不正确的是( )| A. | 还原性HSO3->I-,氧化性:IO3->SO42->I2 | |
| B. | 当a=1时,溶液中n(I2):n(I-)=3:5 | |
| C. | AB段,反应的离子方程式为:IO3-+5I-+6H+═3I2+3H2O | |
| D. | l<a<1.2时,溶液中SO42-与I-的物质的量之比为3:(6-5a) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热蒸发皿和烧杯必须垫石棉网 | |
| B. | 用NaOH溶液滴定醋酸溶液,加入甲基橙作指示剂 | |
| C. | 将硫酸铜溶液蒸发浓缩、冷却结晶得到CuSO4•5H2O | |
| D. | 将一定质量的AlCl3加入到容量瓶中加水定容,配制一定浓度的AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 正在研制的一种“高容量、低成本”锂-铜空气燃料电池,该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )
正在研制的一种“高容量、低成本”锂-铜空气燃料电池,该电池通过一种复杂的铜腐蚀现象产生电力,其中放电过程2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 放电一段时间后右侧睡溶液pH升高 | |
| B. | 整个反应过程中,铜相当于催化剂 | |
| C. | 通空气时,铜被腐蚀,表面产生CuO | |
| D. | 放电时,正极的电极反应式为 Cu2O+H2O+2e-=Cu+2OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com