
【题目】室温下,用0.1 mol·Lˉ1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol·Lˉ1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图,下列说法不正确的是
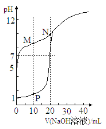
A.HX为弱酸
B.M点c(HX)-c(X-)﹥c(OH-)-c(H+)
C.将P点和N点的溶液混合,呈酸性
D.向N点的溶液中通入HCl至pH=7:c(Na+) ﹥c(HX) = c(Cl-) ﹥c(X-)
【答案】C
【解析】
试题分析:A.未滴定时,0.1molL-1HCl溶液pH为1,由图可知0.1mol/L HX溶液的pH>5,则HX弱酸,故A正确;B.M点为等浓度NaX、HX混合溶液,且溶液呈碱性,说明X-的水解程度大于HX的电离程度,由物料守恒可知:2c(Na+)=c(X-)+c(HX),结合电荷守恒c(Na+)+c(H+)=c(X-)+c(OH-),联立可得:c(X-)+c(HX)+2c(H+)=2c(X-)+2c(OH-),整理得:c(HX)-c(X-)=2c(OH-)-2c(H+)>c(OH-)-c(H+),故B正确;C.P点溶液中NaCl、HCl物质的量相等,N点为NaX溶液,NaX物质的量为HCl的2倍,混合后为NaCl、NaX、HX混合溶液,且溶液中NaX与HX的浓度相等,由于X-的水解程度大于HX的电离程度,呈碱性,故C错误;D.根据电荷守恒:c(Na+)+c(H+)=c(Cl-)+c(X-)+c(OH-),溶液pH=7,则c(Na+)=c(Cl-)+c(X-),由物料守恒可知c(Na+)=c(X-)+c(HX),联立可得c(HX)=c(Cl-),而溶液为NaCl、NaX、HX的混合溶液,相同浓度下X-的水解程度大于HX的电离程度,由于溶液为中性,则溶液中c(NaX)<c(HX),故溶液中c(Na+)>c(HX)=c(Cl-)>c(X-),故D正确;故选C。


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】在下图所示的物质转化关系中,A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,且两种元素化合价的绝对值相等。常温下,C、F、K是无色无味的气体单质,D、H是固体单质。E是常见的两性氧化物。B、G是汽车尾气中的主要污染气体,所含元素均为第二周期元素。反应②常用于汽车尾气的处理。
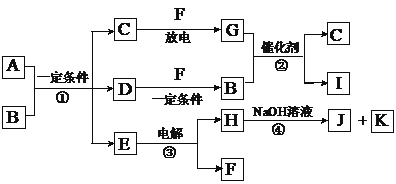
(1)C的电子式 。
(2)A的化学式 。
(3)反应③的化学方程式 。
(4)反应④的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫做活化能,其单位通常用kJ/mol表示。请认真观察下图,然后回答问题:
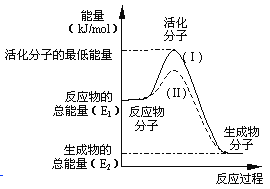
①图中所示反应是__________(填“吸热”或“放热”)反应,该反应____________(填“需要”或“不需要”)加热,该反应的△H=____________(用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+1/2O2(g)=H2O(g);△H=-241.8 kJ/mol。该反应的活化能为167.2kJ/mol,则其逆反应的活化能为____________。
③对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率明显加快,你认为最可能的原因是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的原子有3个电子层,最外层有4个电子.这种元素位于周期表的( )
A.第4周期ⅢA族
B.第4周期ⅦA族
C.第3周期Ⅳ族
D.第3周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物说法正确的是
A. C7H8与C6H6互为同系物
B. 由乙酸与乙醇制备乙酸乙酯的反位属于加成反位
C. C3H6Br2有4种同分异构体
D. 油脂在人体内最终分解为甘油和高级脂肪酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数。
甲方案:
实验步骤为:①称量空坩埚的质量为A g
②称量装有试样的坩埚质量为B g ③加热
④冷却⑤称量坩埚和残余物的质量为C g
⑥重复③至⑤操作,直至恒重,质量为D g
(1)坩埚中发生反应的化学方程式为__________________。
(2)计算Na2CO3质量分数必须用到的测定数据为___________(填“A”、“B”、“C”或“D”)。
乙方案:
在天平上准确称取0.3000 g样品,放入锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用0.1000 mo1·L-1,的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为NaHCO3。重复上述操作两次,消耗盐酸的体积为20.00 mL。
(3)配制上述盐酸标准溶液100 mL,若用2.0 mol·L-1HCl进行配制,需用滴定管量取该HCl溶液________mL;定容时俯视刻度线,将导致配制的溶液浓度___________(填“偏高”、“偏低”或“没有影响”)。
(4)样品中Na2CO3的质量分数为___________(用百分数表示,精确到0.1%)。
丙方案:
称取m g样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
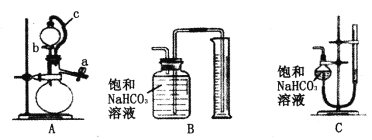
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若装置不漏气,则观察到的现象为__________________。实验时,装置A中c的作用_____________、_____________。
(6)为了提高测定的准确性,应选用装置A和__________(填写字母标号)进行实验。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com