
| 实验操作 | 现象 | 结论 | |
| A | 淀粉溶液中加入碘水 | 溶液变蓝 | 说明淀粉没有水解 |
| B | 将乙醇与酸性重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 蔗糖溶液中加入稀硫酸,水解后加入银氨溶液,水浴加热 | 未出现银镜 | 水解的产物为非还原性糖 |
| D | 将新制Cu(OH)2与葡萄糖溶液混合加热 | 产生红色沉淀(Cu2O) | 葡萄糖具有氧化性 |
| A、A | B、B | C、C | D、D |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
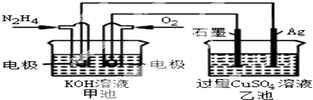
| A、反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度 |
| B、甲池中负极反应为:N2H4-4e-═N2+4H+ |
| C、甲池溶液pH不变,乙池溶液pH减小 |
| D、甲池中消耗2.24L O2,此时乙池中理论上最多产生12.8g固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、39K+和40Ca2+微粒中的电子数和中子数都相等 |
| B、在标准状况下,若D2和He体积相等,则质量不相等 |
| C、7.8g Na2O2与足量的CO2反应时失去的电子数为0.2 NA |
| D、把1mol NaCl溶于1L水中,所得NaCl溶液的物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用食醋可以除去暖水瓶中的薄层水垢 |
| B、用镊子取出白磷并置于水中切割 |
| C、硝酸溶液通常保存在棕色试剂瓶中,是因为硝酸见光易分解 |
| D、常温下浓硫酸可贮存在铁制或铝制容器中,说明常温下铁和铝与浓硫酸不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性.请根据图示判断下列有关说法不正确的是( )
如图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性.请根据图示判断下列有关说法不正确的是( )| A、甲池是原电池、乙池是电解池 |
| B、通入乙醇的惰性电极的电极反应式为:C2H5OH+16OH--12e-═2CO32-+11H2O |
| C、反应一段时间后,两池溶液的pH均未变化 |
| D、假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
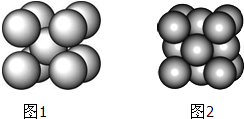 某金属(A)在TK以下晶体的基本结构单元如图1所示,T K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的A原子间距离相同
某金属(A)在TK以下晶体的基本结构单元如图1所示,T K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的A原子间距离相同| 金属 | 相对原子质量 | 分区 | 原子半径/pm | 密度/g?cm-3 | 原子化热/kJ?mol-1 |
| Na | 22.99 | s区 | 186 | 0.960 | 108.4 |
| A | 60.20 | d区 | r | 7.407 | 7735 |
| 3 |
| 200 |
| 27 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 操 作 | 现 象 |
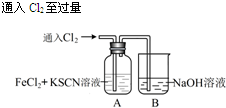 |
I.A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com