
| A、1:1:1 |
| B、1:2:3 |
| C、2:3:5 |
| D、5:3:2 |
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 3 |
| 5 |
| 4 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 5 |
| 4 |


科目:高中化学 来源: 题型:
| 3 |
| 2 |
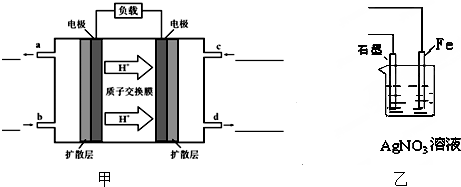
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③⑥ |
| C、②③⑥ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL lmol/L的FeCl3溶液完全生成Fe(OH)3胶体,其胶粒数目为0.1NA |
| B、7.8 g Na2O2中含有的离子总数目为0.4NA |
| C、30g SiO2晶体中含有Si-O键的数目为2NA |
| D、1 L 0.1 mol/L NaHCO3溶液含有0.1nA个HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
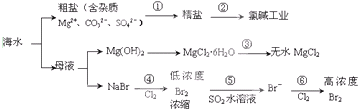
| A、过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B、在过程③中将MgCl2?6H2O灼烧即可制得无水MgCl2 |
| C、在过程④、⑥反应中每氧化0.2 mol Br- 需消耗0.1mol Cl2 |
| D、过程⑤在生产中无需解决其对金属设备的腐蚀问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:
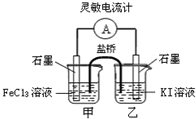 控制适当的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列判断正确的是( )
控制适当的条件,将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列判断正确的是( )| A、反应开始时,乙中电极反应为2I-+2e-=I2 |
| B、反应开始时,甲中石墨电极上发生氧化反应 |
| C、电流表指针为零时,两池溶液颜色相同 |
| D、平衡时甲中溶入FeCl2固体后,乙池的石墨电极为正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com