
【题目】下列离子在指定溶液中一定能大量共存的是
A.加入Al能放出H2的溶液中:Fe2+、K+、NO![]() 、Cl-
、Cl-
B.在pH=13的溶液中:Na+、AlO2-、NO![]() 、S2-、SO
、S2-、SO![]()
C.由水电离的c(H+)=10-12mol·L-1的溶液中:Cl-、NO![]() 、NH
、NH![]() 、F-
、F-
D.NaHCO3溶液中:K+、Na+、SO![]() 、Al3+
、Al3+
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】在反应3NO2+H2O===2HNO3+NO中,发生还原反应和发生氧化反应的物质质量之比为( )
A.3∶1 B.1∶3 C.1∶2 D.2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
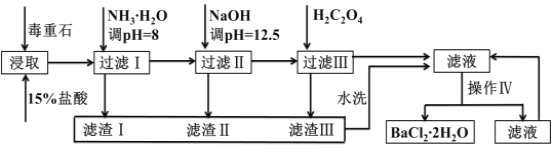
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如下:
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀的pH | 11.9 | 9.1 | 1.9[ |
完全沉淀的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)= 1.6×10–7,Ksp(CaC2O4)= 2.3×10–9
(1)实验室用37%的盐酸配制1mol/L盐酸,下列仪器中,不需要使用的是_______ __
a.容量瓶 b.量筒 c.烧杯 d.滴定管
为了加快毒重石的酸浸速率,可以采取的措施有______________(至少两条)。
(2)加入氨水调节溶液pH=8的目的是___________________________。滤渣Ⅱ中含________(填化学式)。加入H2C2O4时应避免过量,原因是___ __ ____________。
(3)操作Ⅳ的步骤是:______ ______、过滤。
(4)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42—+2H+=Cr2O72—+H2O ;Ba2++CrO42— =BaCrO4↓
步骤Ⅰ:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
通过计算,氯化钡溶液浓度为___________mol·L-1(用含字母的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离的c(H+)=1×10-11mol/L-1,该溶液中的溶质可能是( )
①二氧化硫水溶液②氯化铵水溶液③硝酸钠水溶液④氢氧化钠水溶液
A. ①④ B. ①② C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池反应的离子方程式为:Zn+2H+=Zn2++H2↑,则下列说法正确的是
A. HNO3可作电解质溶液 B. 电子从正极沿导线流向负极
C. 锌极质量不变 D. 石墨可作原电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列叙述正确的是(C-12 H-1)
A.标准状况下,22.4LCCl4所含的分子数为NA
B.1mol的羟基(-OH)与1 mol的氢氧根(OH - )离子所含电子数均为9 NA
C.常温常压下,在30g 的乙烷气体分子中,碳氢键的总个数为6NA
D.一定条件下,将2molSO2与足量的O2充分反应,生成SO3的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质属于常见氧化剂的一组是( )
A. Cl2、O2、FeCl3、KMnO4
B. O2、KMnO4、C、H2
C. Na、K、FeCl2、H2、CO
D. CuO、CO、Fe2O3、H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol碳在氧气中完全燃烧生成气体,放出393kJ的热量,下列热化学方程式表示正确的是
A. C(s)+O2(g)→CO2(g)+393kJ
B. C + O2→ CO2+393kJ
C. C (s) + O2 (g)→CO2 (g)-393kJ
D. C (s) +1/2O2 (g) → CO(g) +393kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com