


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
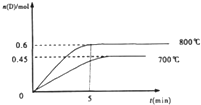 2L容积不变的密闭容器中,加入1.0molA和2.2molB,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图,试回答下列问题:
2L容积不变的密闭容器中,加入1.0molA和2.2molB,进行如下反应:A(g)+2B(g)?C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属元素的原子只有还原性,离子只有氧化性 |
| B、金属单质在常温下均是固体 |
| C、金属元素能存在于阳离子中,而不能存在于阴离子中 |
| D、金属元素在化合物中一定显正价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCHO分子中既含σ键又含π键 |
| B、CO2分子中的化学键为非极性键 |
| C、NH3分子中N原子的杂化轨道类型是sp2 |
| D、沸点:HF>NH3>H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 3 |
| A、85.5% |
| B、66.7% |
| C、33.3% |
| D、27.4% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com