
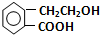 ,它可通过不同化学反应分别制得B、C、D三种物质.
,它可通过不同化学反应分别制得B、C、D三种物质.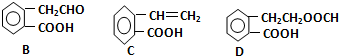
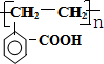 .
. .
. 分析 (1)A中醇羟基被催化氧化生成B中醛基;A中醇羟基发生消去反应生成C中碳碳双键;A中醇羟基发生酯化反应生成D中酯基;
(2)C中碳碳双键在一定条件下能发生加聚反应生成高分子化合物;
(3)A中醇羟基发生催化氧化生成B中醛基.
解答 解:(1)A中醇羟基被催化氧化生成B中醛基;A中醇羟基发生消去反应生成C中碳碳双键;A中醇羟基发生酯化反应生成D中酯基,所以反应的类型:A→B、A→C、A→D分别是催化氧化、消去、酯化,故答案为:催化氧化;消去;酯化;
(2)高聚物为C发生加聚反应的产物,则高聚物的结构简式为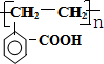 ,故答案为:
,故答案为: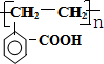 ;
;
(3)A中醇羟基发生催化氧化生成B中醛基,该反应为 ,
,
故答案为: .
.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确官能团之间的转化及反应条件是解本题关键,知道常见官能团结构及其性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验设计或操作 | 观察或记录 | 结论或解释 |
| A | 将某有机物滴入高锰酸钾溶液中 | 高锰酸钾溶液褪色 | 该有机物一定含不饱和键 |
| B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸不反应 |
| C | 向某淡黄色试液X中滴加少许NaOH溶液 | 试液X中出现红褐色沉淀 | 说明试液X中一定含有FeCl3 |
| D | 向装有少许无水硫酸铜的试管中加入乙醇 | 固体由白变蓝 | 该乙醇中一定含有水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:实验题
粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
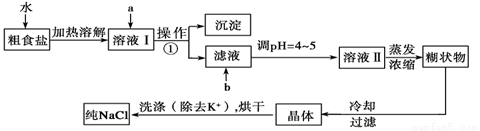
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳、稀盐酸。
(1)欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为___________(只填化学式)。
(2)如何检验SO42-是否沉淀完全_____________。
(3)调节pH的目的是_____________,试剂b是________(填名称)。
(4)洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为______________,使用该试剂的目的是除去晶体表面的杂质,减少晶体的损耗。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使溴水褪色 | B. | 能与新制Cu(OH)2悬浊液反应 | ||
| C. | 与足量的氢气反应生成1-丙醇 | D. | 不能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
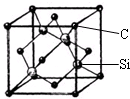 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,若使用催化剂,反应过程中放出的热量更多 | |
| B. | CO燃烧的热化学方程式为2CO(g)+O2(g)=2CO2(g)△H=+285.8kJ/mol | |
| C. | 反应2Mg+CO2=2MgO+C△H<0从熵变角度看,不可自发进行 | |
| D. | 在密闭容器中,2HI(g)?H2(g)+I2(g)△H=+14.9kJ/mol,若投入NA个HI分子,反应平衡时,吸热7.45kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
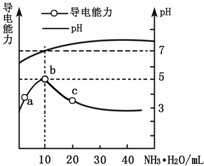 常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )
常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的氨水,所得溶液pH及导电性变化如图.下列分析不正确的是( )| A. | b点溶液pH=5,此时酸碱恰好中和 | |
| B. | a~b点导电能力增强,说明HR为弱酸 | |
| C. | c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | |
| D. | b~c任意点溶液均有c(H+)•c(OH-)=KW=1.0×10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、SO42-、Cl- | B. | Mg2+、K+、Cl-、NO3- | ||
| C. | H+、K+、CO32-、NO3- | D. | Ag+、Ca2+、Cl-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com