
 元素周期表第ⅤA族元素包括氮、磷、砷(As)、锑(Sb)等.这些元素无论在研制新型材料,还是在制作传统化肥、农药等方面都发挥了重要的作用.
元素周期表第ⅤA族元素包括氮、磷、砷(As)、锑(Sb)等.这些元素无论在研制新型材料,还是在制作传统化肥、农药等方面都发挥了重要的作用.分析 (1)N4中氮原子的轨道杂化方式为sp3,其空间构型与P4(白磷)相似;
(2)砷位于第四周期ⅤA族,其最外层电子排布式为4s24p3;
(3)同主族元素从上到下,元素的电负性逐渐减小;
(4)原子数相同,价电子数相同的微粒互为等电子体;
(5)有机物分子中C原子连接4个不同的原子或原子团,则该分子存在手性异构体;
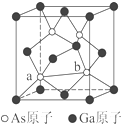
(6)计算出晶胞中微粒数,利用ρ=$\frac{m}{V}$计算;a位置As原子与b位置As原子之间的距离为晶胞立方体体对角线的一半.
解答 解:(1)N4中氮原子的轨道杂化方式为sp3,其空间构型与P4(白磷)相似,空间构型应为正四面体结构,N-N键的键角为60°;
故答案为:正四面体;60°;
(2)砷为33号元素,位于第四周期ⅤA族,其最外层电子排布式为4s24p3;
故答案为:4s24p3;
(3)同主族元素从上到下,元素的电负性逐渐减小,则电负性:N>P>As;
故答案为:N>P>As;
(4)原子数相同,价电子数相同的微粒互为等电子体,则与N3-互为等电子体的微粒有CO2或CS2或N2O等;
故答案为:CO2或CS2或N2O;
(5)有机物分子中C原子连接4个不同的原子或原子团,则该分子存在手性异构体,HOCH2CH(NH2)COOH分子中第二个碳原子属于手性碳原子,则该分子存在手性异构体;
故答案为:是;
(6)晶胞中Ga原子数为6×$\frac{1}{2}$+8×$\frac{1}{8}$=4,As原子数为4,则ρ=$\frac{m}{V}$=$\frac{\frac{75×4+70×4}{{N}_{A}}}{(c×1{0}^{-10})^{3}}$=$\frac{5.8×1{0}^{32}}{{N}_{A}•{c}^{3}}$g•cm-3;a位置As原子与b位置As原子之间的距离为晶胞立方体体对角线的一半,则两原子之间的距离为$\frac{1}{2}$$\sqrt{{c}^{2}+{c}^{2}}$=$\frac{\sqrt{2}}{2}$cpm;
故答案为:$\frac{5.8×1{0}^{32}}{{N}_{A}•{c}^{3}}$;$\frac{\sqrt{2}}{2}$c.
点评 本题考查学生对物质结构与性质模块的掌握情况,涉及电负性、电子排布、空间结构、等电子体、晶胞的有关计算等,考查知识全面、覆盖广,难度适中,可以衡量学生对该模块主干知识的掌握情况.


科目:高中化学 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:选择题
对下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
A.0.1mol•L-1(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-)
B.0.1mol•L-1NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-)
C.0.2mol•L-1NaA溶液和0.1mol•L-1盐酸等体积混合所得溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.25℃100mL0.1mol•L-1的NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3·H2O)
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三上学期期中考试化学试卷(解析版) 题型:选择题
某恒温密闭容器发生可逆反应Z(?)+W(?) X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是

A.Z和W在该条件下至少有一个是为气态
B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大
D.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三上学期期中考试化学试卷(解析版) 题型:选择题
已知某有机物A分子式为C5H10O2,且能与NaHCO3溶液反应产生气体,则A的同分异构体数目共有(不考虑立体结构)
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
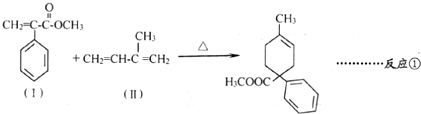
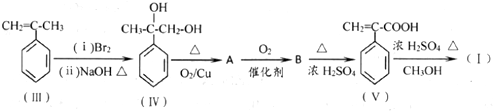
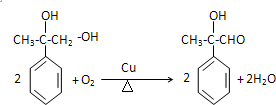 .
. 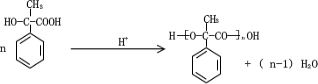 .
.  .
. 和其他无机物叫合成
和其他无机物叫合成 ,最合理的方案
,最合理的方案 $→_{催化剂}^{H_{2}}$
$→_{催化剂}^{H_{2}}$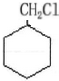 $→_{△}^{NaOH、醇}$
$→_{△}^{NaOH、醇}$ $\stackrel{Cl_{2}}{→}$
$\stackrel{Cl_{2}}{→}$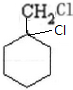
 .
. 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
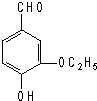
| A. | 1 mol乙基香草醛最多可与1 mol氢气发生加成反应 | |
| B. | 乙基香草醛可与Br2的CCl4溶液发生加成反应 | |
| C. | 1mol乙基香草醛可与含3 mol NaOH的水溶液完全反应 | |
| D. | 乙基香草醛能被酸性高锰酸钾、银氨溶液、新制的氢氧化铜等氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于Si+O2═SiO2,每当新形成2NA个Si-O键,需要断开NA个Si-Si键 | |
| B. | 12.0g熔融的NaHSO4中含有的阳离子数为0.1NA | |
| C. | 次氯酸光照分解产生22.4mL气体(标准状况)转移的电子数为0.002NA | |
| D. | 电解精炼铜时,若阴极析出32g铜,则转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com