
【题目】既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是:
A. 在空气中燃烧 B. 通入足量溴水中
C. 通入酸性高锰酸钾溶液中 D. 通入水中
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为![]() ,溶质的质量分数为ω,溶质的物质的量浓度为C mol/L。下列叙述中正确的有( )
,溶质的质量分数为ω,溶质的物质的量浓度为C mol/L。下列叙述中正确的有( )
①![]() ②
②![]() ③上述溶液中加入V mL水后,所得溶液的质量分数大于0.5ω ④上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
③上述溶液中加入V mL水后,所得溶液的质量分数大于0.5ω ④上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
A. ②③ B. ②④ C. ③④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的酸性由强到弱排列正确的是
A.碳酸、甲酸、乙酸、苯酚B.乙酸、甲酸、碳酸、苯酚
C.甲酸、碳酸、乙酸、苯酚D.甲酸、乙酸、碳酸、苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 常温下,加水稀释醋酸,![]() 增大
增大
C. 多元弱酸的酸性主要由第一步电离决定
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应aA(g)+bB(s)cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )

A. 根据图象无法确定改变温度后平衡移动方向
B. 使用催化剂,C的物质的量分数增加
C. 化学方程式系数a>c+d
D. 升高温度,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对金属及其制品的防护措施中,错误的是
A.把Cr、Ni等金属加入到普通钢里制成不锈钢铁
B.通过特殊工艺,增加铝制品表面的氧化膜
C.对于易生锈的铁制品要定期刷防护漆
D.锅用完后,用水刷去其表面的油污,置于潮湿处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用硫酸烧渣(主要成分Fe2O3、FeO、Fe3O4、FeS2、SiO2)制备铵黄铁矾[(NH4)xFey(SO4)z(OH)n,其中Fe为+3价]的工艺流程如下:
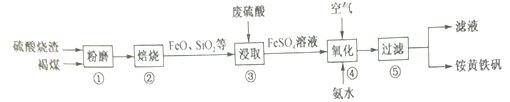
回答下列问题:
(1)焙烧前需进行“粉磨”的目的是_______________;硫酸烧渣加褐煤高温焙烧的主要目的是__________。
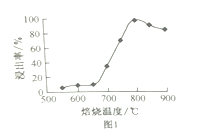
(2)“焙烧”的温度与“浸取”时浸出率的关系如下图1所示,超过800℃时,浸出率开始降低,其原因是缺少_____________________;
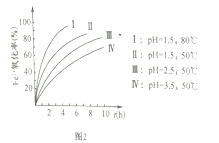
(3)步骤④Fe2+的氧化率随控制条件及时间的变化关系如上图2所示,适宜的条件为 _________选填I、II、III、IV)。从滤液中可回收的产品是________________(填化学式)。
(4)为测定产品铵黄铁矾的化学式,进行以下实验:
步骤1:取19.2 g铵黄铁矾,加足量的稀盐酸溶解,将所得溶液分为A、B两等份;
步骤2:向A中加入足量的NaOH溶液并加热,共收集到0.448L NH3(标准状况下)过滤后将所得滤渣洗涤干燥并灼烧至质量不再变化,可得4 8 g固体残渣;
步骤3:向B中加入足量的BaCl2溶液,过滤洗涤干燥,可得9. 32 g固体残渣。
则产品铵黄铁矾的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如图装置与操作以替代相关的实验.实验操作:钠与氯气反应的装置可作如右图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球.先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟.以下叙述中错误的是( ) 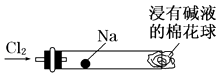
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C.钠着火燃烧产生苍白色火焰
D.发生的反应为2Na+Cl2═2NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com