
| A. | 反应CO(g)+NO2(g)?CO2(g)+NO(g),△H<0,达到平衡后,升高温度系颜色变深 | |
| B. | 高压比常压有利于SO2与O2合成SO3的反应. | |
| C. | 加入催化剂有利于N2与H2合成NH3的反应 | |
| D. | 工业制取金属钾[Na(l)]+KCl(l)?NaCl(l)+K(g)]选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A、反应CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度平衡逆向移动,体系颜色变深,能用勒夏特列原理解释,故A不选;
B、高压有利于SO2与O2合成SO3的化学平衡正向移动,能用勒夏特列原理解释,故B不选;
C、因催化剂对化学平衡移动无影响,则采用催化剂不改变平衡,不能用勒夏特列原理解释,故C选;
D、工业制取金属钾Na(l)+KCl(l)?NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来,平衡正向进行,反应顺利进行,能用勒夏特列原理解释,故D不选.
故选C.
点评 本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆反应.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)中和热测定实验中,用到的玻璃仪器有烧杯、温度计、环形玻璃搅拌棒、量筒
(1)中和热测定实验中,用到的玻璃仪器有烧杯、温度计、环形玻璃搅拌棒、量筒查看答案和解析>>
科目:高中化学 来源: 题型:解答题
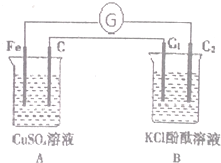 按图装置进行试验时,观察到电流指针发生偏转,B池中C2极区溶液变红,回答下列问题(C,C1,C2均为石墨电极)
按图装置进行试验时,观察到电流指针发生偏转,B池中C2极区溶液变红,回答下列问题(C,C1,C2均为石墨电极)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
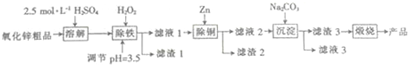
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe2+ | 6.4 | 8.4 |
| Fe3+ | 2.7 | 3.2 |
| Cu2+ | 5.2 | 6.7 |
| Zn2+ | 6.8 | 9.0 |
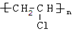 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | U原子核中含有92个中子 | B. | U原子核外有143个电子 | ||
| C. | 23592U和23892U互为同位素 | D. | 23592U和23892U互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com