
| 温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
| A、T1>T2,且a>0 |
| B、当温度为T2、反应进行到40 min时,x>0.15 |
| C、温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)=0.70mol |
| D、温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50 molH2O(g),反应开始时,ν(正)>ν(逆) |
| c2(H2O)?c(CO2)?c(N2) |
| c(CH4)?c2(NO2) |
| 0.82×0.4×0.4 |
| 0.1×0.42 |
| c2(H2O)?c(CO2)?c(N2) |
| c(CH4)?c2(NO2) |
| 0.52×2.0×1.0 |
| 0.50×0.502 |


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
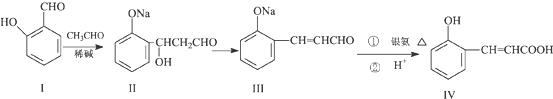
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| C(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
| 实验编号 | T/℃ | NO初始浓度/mol?L-1 | CO初始浓度/mol?L-1 | 催化剂的比表面积/m2?g-1 |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9:1 | B、18:7 |
| C、41:9 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+4价 | B、+5价 |
| C、+6价 | D、+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液的pH增大 |
| B、溶液中的H+向锌电极定向移动 |
| C、锌电极的反应为2H++2e-=H2↑ |
| D、外电路中,电子由铜电极转移到锌电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质类别 | 强酸 | 强碱 | 酸式盐 | 氧化物 | 氢化物 |
| 化学式 | ①HNO3 ② | ③NaOH ④ | ⑤NaHSO4 ⑥ | ⑦SO2 ⑧SO3 | ⑨NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com