
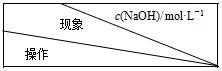
 | 5.0 | 6.0 | 7.0 |
| ʵ����뼸��KSCN��Һ | ����� | ����� | ����� |
| ʵ����ȼ������ϡ���ᣬ�ٵ��뼸��KSCN��Һ | ����� | ��� | ��� |
���� ��1����������������������������������������
�����Ի�������FeO2-��c��NaOH����6.0 mol•L-1ʱ�����������ӣ���KSCN��Ӧ��
��2����̼���������ᷴӦ���ɶ�����̼�������ɣ�
��������������������ӷ���������ԭ��Ӧ�õ��������ӣ��������������ƣ��õ�FeSO3��
��3�����ݾ����ܵõ������IJ�Ʒ�Ƚ����ַ����ɵã�
��4��FeSO4��Һ����NaClO��Fe��OH��3��
��� �⣺��1���ٲ������ɫ���������ӷ���ʽ��Fe3++3OH-?Fe��OH��3�����ʴ�Ϊ��Fe3++3OH-?Fe��OH��3����
�����Ի����£�����FeO2-��ʽ���ڣ���c��NaOH����6.0 mol•L-1ʱ��FeO2-+4H+?Fe3++2H2O��������ʹKSCN�Ժ�ɫ��Fe3++3SCN-?Fe��SCN��3��
�ʴ�Ϊ��FeO2-+4H+?Fe3++2H2O��Fe3++3SCN-?Fe��SCN��3��
��2����̼���������ᷴӦ���ɶ�����̼�������ɣ�֤�������к���̼���οɼ�������ϡ���ᣬ����ɫ���������
�ʴ�Ϊ����������ϡ���ᣬ����ɫ���������
����1mL 1.0mol•L-1FeCl3��Һ�еμ�1.0mol•L-1Na2SO3��Һ������Ӧ��2Fe3++SO32-+H2O?2Fe2++SO42-+2H+�������μ�Na2SO3��Һ��Fe2++SO32-?FeSO3����
�ʴ�Ϊ��2Fe3++SO32-+H2O?2Fe2++SO42-+2H+��Fe2++SO32-?FeSO3����
��3����2�����������������ʣ����ף���1������������Ũ�ȹ��������ӵ������ʲ��ߣ���ѡ��1mL 1.0 mol•L-1 FeCl3��Һ��3 mLŨ��С��6.0 mol•L-1��NaOH��Һ��
�ʴ�Ϊ��1 mL 1.0 mol•L-1 FeCl3��Һ��3 mLŨ��С��6.0 mol•L-1��NaOH��Һ��
��4��FeSO4��Һ����������NaClO��Fe��OH��3���ʴ�Ϊ��NaClO��
���� ���⿼���������������й����ʣ��漰������ԭ��Ӧ�����ʵ��Ʊ���ʵ��������ѡ���֪ʶ�㣬��Ŀ�Ѷ��еȣ�Ҫ��ѧ�������ʻ���֪ʶ�����գ�������Ŀ��Ϣ������ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��MnO4-��Cl-��SO42- | B�� | Na+��CO32-��SO42-��Cl- | ||
| C�� | NO3-��Na+��HCO3-��Ba2+ | D�� | Na+��NO3-��H+��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҵ�ϳɰ�ʱʹ�ô��� | |
| B�� | ����SnCl2��Һʱ����һ���������� | |
| C�� | 25��ʱ����ϡ������Һ����ˮ�������c��H+����1��10-7mol/L | |
| D�� | AgCl��ˮ�е��ܽ�ȴ����ڱ���NaCl��Һ�е��ܽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ʼ��������mol�� | ƽ��ʱ | ||||
| A | B | C | A��Cת���ʣ�%�� | C�����ʵ���������%�� | �ų�������������KJ�� |
| 1 | 1 | 0 | ��1 | ��1 | Q1 |
| 0 | 0 | 2 | ��2 | ��2 | Q2 |
| 2 | 2 | 0 | ��2 | ��3 | Q3 |
| A�� | ��1+��2=1����2=��1 | B�� | ��3=2��1��Q3=2Q1 | C�� | ��3=��1=��2��Q3=2Q1 | D�� | ��1=��3��Q1+Q2=Q |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
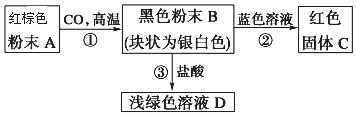
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
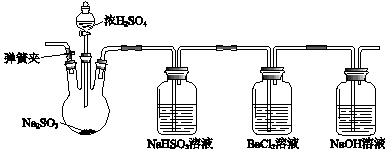
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.2mol | B�� | 0.1mol | ||
| C�� | ��0.1mol | D�� | ����0.1mol����0.2mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | A | B | C | D | E |
| ԭ�Ӱ뾶/pm | 160 | 143 | 102 | 56 | 117 |
| ��Ҫ���ϼ� | +2 | +3 | +6��+4��-2 | -1 | +6��+4��-2 |
| A�� | Ԫ��A��B�������������������ͻ���� | |
| B�� | ��Ԫ��B��C��ɵĻ��������ͨ�������뵥�ʻ����Ƶã�Ҳ��������Һ��ͨ�����ֽⷴӦ�Ƶ� | |
| C�� | ��̬�⻯��Ļ�ԭ�ԣ�C��E | |
| D�� | DԪ�صķǽ�������ǿ��������������Ӧˮ�����������ǿ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com