
欲检验CO2气体中是否含有SO2、HC1,进行如下实验:
①将气体通入酸化的AgNO3溶液中,产生白色沉淀a;
②滤去沉淀a,向滤液中加入Ba(NO3)2溶液,产生白色沉淀b。
下列说法正确的是 ( )
A.沉淀a为AgC1 B.沉淀b为BaCO3 C.气体中含有SO2 D.气体中没有HC1
科目:高中化学 来源: 题型:
无水氧化亚铁用于制造铁系催化剂、印染的媒染剂和染料还原剂,还可用于冶金、医药、照相等行业。一实验小组模仿工业方法制取氯化亚铁,设计装置如下
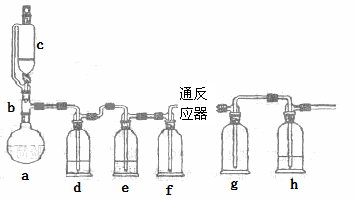

通过查阅相关资料可知:
①在持续高温500℃时,铁与纯净、干燥Cl2反应可生成FeCl2,在温度较低时可生成FeCl3;
②FeCl3熔沸点低,易升华。
根据以上信息回答相关的问题
(1)abc仪器组合成制取氯气的装置,反应无需加热,请写出a溶器内所发生的化学反应方程式 。
(2)d、e盛装的药品分别是 和 ,f、g的作用是 。
(3)反应器为硬质玻璃管,纯净铁粉与氯气在500℃左右反应。
①化学反应方程式为
②实验操作顺序是:组装仪器、 、装入药品、 、
、停止加热、关闭c的活塞。
(4)实验小组记录的实验现象如下:
| 观察到的部分现象 | |
| 第一次实验 | 反应器中有白雾、红色固体、g瓶有白雾和黄绿色气体 |
| 第二次实验 | 反应器中有绿色晶体,g瓶有红棕色的烟和黄绿色气体 |
| 第三次实验 | 反应器中有绿色晶体,g瓶有黄绿色气体 |
①第一次实验,发现e瓶没有盛装任何药品,所以得到红色固体,其原因是 。
②第二次实验,g瓶有红棕色的烟,其原因是 。
(5)第三次实验得到的固体,最可能含有微量杂质是 ,如果需要配制约2~3mol/L的染料还原剂溶液,则无需除去,理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1~18号元素的离子aX m+、bY n+、cZP-、dWk-都具有相同的电子层结构,下列关系正确的是
A.若P>K,则还原性cZP- <dWk-
B.若m > n, 则碱性 X(OH)m > Y(OH)n
C.若半径aX m+>bY n+ ,则a<b
D.若半径aX m+ > bY n+ ,则X的单质一定能从含Y n+ 的盐溶液中置换出Y
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式的书写中,正确的是 ( )
A.铁与盐酸反应: 2Fe+6H+===2Fe3++3H2↑
B. NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-= NH3↑+H2O
C.AlCl3溶液中加入足量的氨水: Al3++ 3OH- ══ Al(OH)3↓
D. 碳酸氢钠溶液中滴入稀盐酸: HCO3- +H+ = CO2 ↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将X和Y 各0.16 mol充入10 L 恒容密闭容器中,发生反应
X(g)+ Y(g)
 2Z(g) △H < 0,反应过程中测定的数据如下表
2Z(g) △H < 0,反应过程中测定的数据如下表
| t / min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是 ( )
A. 反应前2min的平均速率v(Z)=2.0×10-5 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案如下:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度和质量相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________________。
(2)甲方案中说明HA是弱电解质的理由是测得溶液的pH______1
(选填“>”、“<”或“=”)。
(3)乙方案中说明HA是弱电解质的现象是 ____。
①装HCl溶液的试管中放出H2的速率快;
②装HA溶液的试管中放出H2的速率快;
③两个试管中产生气体的速率一样快。
(4)请你评价:乙方案中难以实现之处和不妥之处:
________________________________________________________________________。
(5)请你提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述:
_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,错误的是
A.H2S、H2O、HF的稳定性依次增强
B.RbOH、KOH、Mg(OH)2的碱性依次减弱
C.Ca、Mg、Na的还原性依次减弱
D.H2SiO3、H2CO3、H2SO4的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在研究化学反应中的能量变化时,做了下面的实验:

在一个小烧杯里,加入20 g已研磨成粉末的Ba(OH)2·8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10 g NH4Cl晶体,根据实验步骤,填写下表,并回答问题。
| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 ① 产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 ② 反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 ③ 生成 |
① ② ③
④写出实验过程中发生反应的化学方程式:____________________。
⑤实验中要立即用玻璃棒迅速搅拌的原因是: __________________。
⑥在上述实验过程中,为什么用浸有稀硫酸的湿棉花置于多孔塑料板上?
______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱 原理制取Na2CO3的流程图。
原理制取Na2CO3的流程图。

已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl。请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。
精制除杂的步骤顺序是a→________→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣 b.加入盐 酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
e.过滤
向饱和食盐水中先通入NH3,后通入CO2,理由是_________________________ _________________________________________________________________。
(2)灼烧固体A制Na2CO3在________(填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是_____________________________________ _________________________________________________________________。
对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+、K+的溶液中加入少量NH4HCO3使pH降低,反应的离子方程式为____________________。
(3)下图装置中常用于实验室制备CO2的是________(填字母编号);用b装置制备NH3,分液漏斗中盛放的试剂是________(填试剂名称),烧瓶内可加入的固体试剂是________(填试剂名称)。
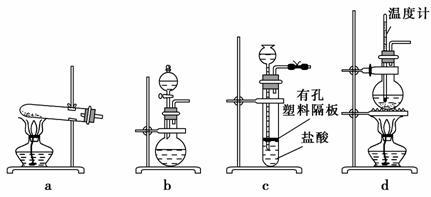
(4)一种天然碱晶体成分是aNa2CO3·bNa2SO4·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实验方案。(仪器自选)请把实验方案填全:
供选择的试剂:1.0 mol·L-1 H2SO4 溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
①称取m1g天然碱晶体样品,溶于适量蒸馏水中。
②_______________________________________________________________。
③_______________________________________________________________。
④计算天然碱晶体中含Na2CO3的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com