
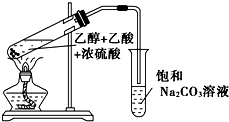
 实验室制备乙酸乙酯,是将3mL乙醇加入一支试管中,然后边振荡试管,边慢慢加入2mL浓H2SO4和2mL乙酸,按如图连接好装置,在酒精灯上加热.观察现象.
实验室制备乙酸乙酯,是将3mL乙醇加入一支试管中,然后边振荡试管,边慢慢加入2mL浓H2SO4和2mL乙酸,按如图连接好装置,在酒精灯上加热.观察现象.分析 (1)乙酸和乙醇在浓硫酸作用下发生酯化反应,生成乙酸乙酯和水;
(2)和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;
(3)催化剂参与化学反应,改变反应历程,降低了正、逆反应的活化能,增大了活化分子的百分数而改变反应速率,不能使原本不能发生的反应得以发生;
(4)开始时用酒精灯对左试管小火加热根据温度对反应速率影响及乙酸乙酯、乙醇、乙酸的沸点进行分析;后改用大火加热根据反应为可逆反应及时蒸出生成的乙酸乙酯,使反应向右进行;
(5)用用饱和食盐水和饱和氯化钙洗涤除去碳酸钠和乙醇,无水硫酸钠吸水形成硫酸钠结晶水合物;不能选择P2O5、碱石灰和NaOH等固体干燥剂,以防乙酸乙酯在酸性(P2O5遇水生成酸)或碱性条件下水解,根据产率=$\frac{实际产量}{理论产量}$×100%计算解答.
解答 解:(1)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯;
故答案为:中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯;
(3)A.催化剂参加化学反应,故错误;
B.催化剂参加化学反应,但反应前后质量和化学性质不会改变,故错误;
C.催化剂参加化学反应,但反应前后质量和化学性质不变,故正确;
D.催化剂可以改变反应速率,不可以改变可逆反应进行的程度,故错误;
E.催化剂是通过改变化学反应途径进而改变活化能,从而改变化学反应速率,故正确.
故选CE;
(4)本实验反应开始时用小火加热,目的是加快反应速率,同时由于反应物乙酸、乙醇沸点较低,小火加热防止反应物为来得及反应而挥发损失,后改用大火加热,只因为反应为可逆反应,及时蒸出生成的乙酸乙酯,使反应向右进行.
故答案为:开始时用小火加热,目的是加快反应速率,同时由于反应物乙酸、乙醇沸点较低,小火加热防止反应物为来得及反应而挥发损失,后改用大火加热,只因为反应为可逆反应,及时蒸出生成的乙酸乙酯,使反应向右进行.
(5)乙酸乙酯中混有碳酸钠和乙醇,用饱和食盐水萃取碳酸钠,用氯化钙除去少量乙醇,用无水硫酸钠除去少量的水,无水硫酸钠吸水形成硫酸钠结晶水合物;不能选择P2O5、碱石灰和NaOH等固体干燥剂,以防乙酸乙酯在酸性(P2O5遇水生成酸)或碱性条件下水解,所以b正确,将3mL乙醇加入一支试管中,然后边振荡试管,边慢慢加入2mL浓H2SO4和2mL乙酸,最后得乙酸乙酯2mL.
CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
60 46 88 18
1.05(g•cm-3)×2mL 3mL×0.79(g•cm-3)
乙醇剩余,乙酸完全反应,得到乙酸乙酯的质量=$\frac{88×1.05×2}{60}$g=3.08g,实际产量=2mL×0.90(g•cm-3)=1.8g,所以产率=$\frac{1.8g}{3.08g}$×100%≈58.4%,故答案为:58.4%.
点评 本题考查了乙酸乙酯的制备方法、可逆反应特点,题目难度中等,注意掌握乙酸乙酯的反应原理及制备方法,明确可逆反应特点,浓硫酸、饱和碳酸钠溶液、长导管在酯化反应中的作用为考查的热点,要求学生熟练掌握.


科目:高中化学 来源: 题型:选择题
| A. | 食盐水、糖水、冰水都属于混合物 | |
| B. | 烧碱、火碱、消石灰都属于碱 | |
| C. | KHSO4、HCl、HNO3在水中都能电离出氢离子,都属于酸 | |
| D. | 溶液、胶体、浊液都属于稳定的分散系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,固体的量减少 | |
| B. | 加入少量Na2CO3粉末能增大钙离子的浓度 | |
| C. | 降低温度,溶液中c(OH-)增大 | |
| D. | 恒温下加入少量CaO,溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
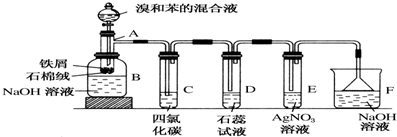
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
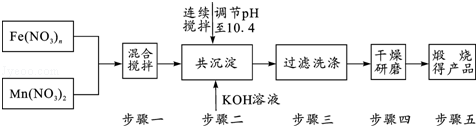
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L水中所含的分子数约为6.02×1023 | |
| B. | 标准状况下,aL的氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$×6.02×1023 | |
| C. | 常温常压下,48g O3气体含有的氧原子数为6.02×1023 | |
| D. | 1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应放出的热量始终小于92.4 kJ | |
| B. | 有无催化剂该反应放出的热量都为92.4 kJ | |
| C. | 在有催化剂存在的条件下,反应放出的热量为92.4 kJ | |
| D. | 若再充入1 mol H2,到达平衡时放出的热量应为92.4 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com