
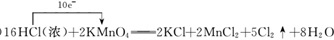 .
.分析 (1)反应中锰元素全部被还原,锰元素化合价由+7价降低为+2价,氯元素化合价由HCl中的-1升高为氯气中的0价,反应电子转移的数目为10e-;
(2)反应中2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,高锰酸钾是氧化剂,浓盐酸部分是还原剂,由此分析解答;
(3)氧化剂的氧化性强于氧化产物的氧化性,所以KMnO4的氧化性比Cl2的氧化性强;
(4)由反应方程式可知:每转移10mol的电子,产生氯气为:5mol,所以反应中每转移2mol电子,产生的Cl2为1mol,由此解答.
解答 解:(1)反应中锰元素全部被还原,锰元素化合价由+7价降低为+2价,氯元素化合价由HCl中的-1升高为氯气中的0价,反应电子转移的数目为10e-,所以电子转移的方向和数目为: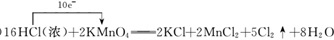 ,故答案为:
,故答案为: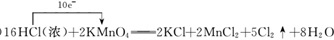 ;
;
(2)反应中2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O,高锰酸钾是氧化剂,浓盐酸部分是还原剂,16mol盐酸中只有10mol的氯的化合价变化,充当还原剂,所以氧化剂与还原剂的物质的量之比是1:5,故答案为:1:5;
(3)氧化剂的氧化性强于氧化产物的氧化性,所以KMnO4的氧化性比Cl2的氧化性强,故答案为:强;
(4)由反应方程式可知:每转移10mol的电子,产生氯气为:5mol,所以反应中每转移2mol电子,产生的Cl2为1mol,所以标况下的体积为:22.4L,故答案为:22.4L.
点评 本题考查氧化还原反应基本概念与计算,难度不大,(3)可以先计算参加反应的HCl,再根据方程式计算生成的氯气,也可利用电子转移守恒计算,根据情况选择.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:实验题
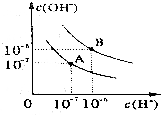 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、苯、环己烷属于脂肪烃 | B. | 苯、环己烷属于芳香烃 | ||
| C. | 乙烯、乙炔属于烯烃 | D. | 环戊烷、环己烷属于环烷烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
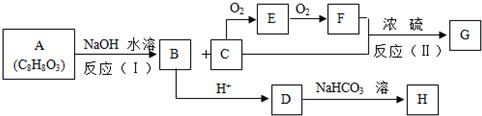
 ,E:HCHO,H:
,E:HCHO,H: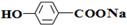 G:HCOOCH3,.
G:HCOOCH3,. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | B. | 气体的总物质的量 | ||
| C. | 消耗1摩尔A同时生成1摩尔D | D. | 混合气体的密度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com