
【题目】在下列变化过程中,既有离子键被破坏又有共价键被破坏的是( )
A.将 SO2 通入水中
B.将 HCl 通入水中
C.烧碱溶于水
D.硫酸氢钾溶于水
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中正确的是
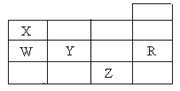
A. 常压下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的氢化物比X的氢化物稳定
D. Y元素最高价氧化物对应水化物比W元素的最高价氧化物对应水化物的酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于分子晶体的说法正确的是
A.晶体中分子间作用力越大,分子越稳定
B.在分子晶体中一定存在共价键
C.冰和Br2都是分子晶体
D.稀有气体不能形成分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
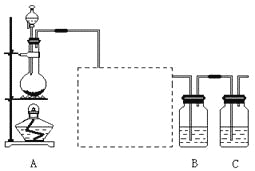
(1)装置A的分液漏斗中盛装的试剂是 ,烧瓶中加入的试剂是 。
(2)虚线框内的实验装置的作用 。
(3)装置B中盛放的试剂是 (选填下列所给试剂的代码),实验现象为 ,化学反应方程式是 ,该反应属于四种基本反应类型中的 _______反应。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体
E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为 ,B为 ,C为 。
(2)写出A、B所形成的化合物与E反应的化学方程式:
(3)A、B两元素形成的化合物属于 (“离子”或“共价”)化合物。
(4)写出D的最高价氧化物的水化物和A单质反应的化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
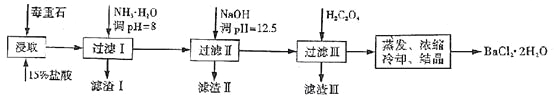
(1)毒重石用盐酸浸取前需充分研磨,目的是 。实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的 。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
加入NH3·H2O调节pH=8可除去 (填离子符号),滤渣Ⅱ中含 (填化学式)。加入H2C2O4时应避免过量,原因是 。
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)利用简洁酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42—+2H+=Cr2O72—+H2O;Ba2++CrO42—=BaCrO4↓
步骤Ⅰ:移取xml一定浓度的Na2CrO4溶液与锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ 相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的 (填“上方”或“下方”)。BaCl2溶液的浓度为 mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将 (填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周辉《清波杂志》卷十二:信州铅山胆水自山下注,势若瀑布,用以浸铜,铸冶是赖,虽干溢系夫旱涝,大抵盛于春夏,微于秋冬。古传一人至水滨,遗匙钥,翌日得之,已成铜矣。这里的胆水是指
A. FeSO4 溶液 B. CuSO4 溶液 C. 氨水 D. NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究。
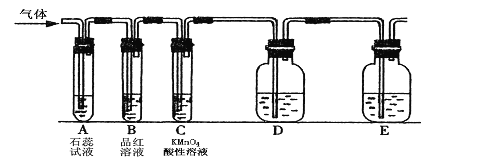
(1)从物质分类的角度,SO2属于________(填“酸性”或“碱性”)氧化物。写出硫酸型酸雨形成的反应方程式: _______ ,_____ 。
(2)图中D装置可用来验证SO2具有该性质,其中所加入的试剂是 _____。
(3)当向该装置通入SO2时,A中紫色石蕊溶液变红,用化学用语解释其原因是 ______ 。
(4)从元素化合价的角度分析,SO2的性质。
①当向该装置通入SO2一段时间后,可观察C中溶液褪色,MnO4-转化为Mn2+,说明SO2具
有______性,反应的离子方程式为 _________。
②如验证SO2还具有另一方面的性质,可选择的药品是__________。
A.过氧化氢 B.浓硫酸 C.氯水 D.硫化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com