
X、Y、Z、W为短周期元素且原子序数依次增大。X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上。Y2-的M能层的原子轨道为全空状态。Z的单质用作铝热反应的引燃剂。 W与X形成的化合物是一种常见的有机溶剂n 。A为第四周期元素,其基态原子含有6个未成对电子。
请回答下列问题:
(1)X在元素周期表中的位置是 。
(2)A3+的外围电子排布式是 。
(3)X、Y、Z形成的晶胞结构示意图如右,则它的化学式是 。
(4)m分子中,X的原子轨道杂化类型是 ,n的分子构型是 。
(5)气体m和含A2Y 的酸性溶液,可通过惰性电极连接构成高能原电池,该电池的正极反应式是 。
的酸性溶液,可通过惰性电极连接构成高能原电池,该电池的正极反应式是 。
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
下列叙述中,错误的是 ( )
A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯
B.苯乙烯在合适条件下催化加氢可生成乙基环己烷
C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
使1mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照条件
下发生取代反应,则两个过程中消耗氯气的总的物质的量是 ( )
A.3mol B.4mol C.5mol D.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
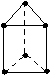 新合成的一种烃,其碳架呈三棱柱体(如图所示)
新合成的一种烃,其碳架呈三棱柱体(如图所示)
(1)该烃的一氯取代物是否有同分异构体
(2)该烃的二氯取代物有多少种
(3)该烃的同分异构体有多种 ,其中一种不能使酸性高锰酸钾溶液或Br2的CCl4溶液褪色,但在一定条件下能跟溴(或H2)发生取代(或加成)反应,这种同分异构体的结构简式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1mol C(金刚石)中含有C—C键的数目为4NA
B.标准状况下,22.4L乙烯中含有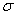 键的数目为5NA
键的数目为5NA
C.含0.2moi H2SO4的浓硫酸与足量铜充分反应,生成SO2分子的数目为0.1NA
D.电解精炼铜时,若阳极质量减少32g,则阴极得到电子的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(白磷,s)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ·mol-1①
P(红磷,s)+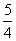 O2(g)===
O2(g)===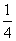 P4O10(s) ΔH2=-738.5 kJ·mol-1②
P4O10(s) ΔH2=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为____________________________。相同状况下,能量状态较低的是________;白磷的稳定性比红磷________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
燃烧热是指1 mol可燃物充分燃烧生成稳定氧化物时放出的热量。已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是-285.8 kJ·mol-1、-1 411.0 kJ·mol-1和-1 366.8 kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的ΔH为( )
A.-44.2 kJ·mol-1 B.44.2 kJ·mol-1
C.-330 kJ·mol-1 D.330 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
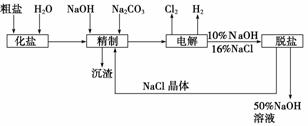
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的电极反应式为________________________,与电源负极相连的电极附近,溶液pH________(选填“不变”、“升高”或“下降”)。
(2)工业食盐中含Ca2+、Mg2+等杂质,精制过程中除去这些杂质时发生反应的离子方程式为________________________________________________________________________、
________________________________________________________________________。
(3)如果粗盐中SO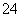 含量过高,必须添加钡试剂除去SO
含量过高,必须添加钡试剂除去SO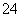 ,该钡试剂可以是________(填写字母序号,下同)。
,该钡试剂可以是________(填写字母序号,下同)。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(4)为有效除去Ca2+、Mg2+、SO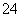 ,加入试剂的合理顺序为________。
,加入试剂的合理顺序为________。
A.先加NaOH,后加Na2CO3,再加钡试剂
B.先加NaOH,后加钡试剂,再加Na2CO3
C.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________
(填写操作名称)除去NaCl。
(6)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜法电解冷的食盐水时,Cl2与NaOH充分接触,得到的产物仅是NaClO和H2,则与该反应相应的化学方程式为________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由浅绿色变为棕黄色。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有 ( )。
A.氧化性 B.还原性
C.碱性 D.酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com