
【题目】二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。现在工业由以下两种方法制备二氧化钛:
方法1:可用含有Fe2O3、SiO2的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要工艺流程如下:
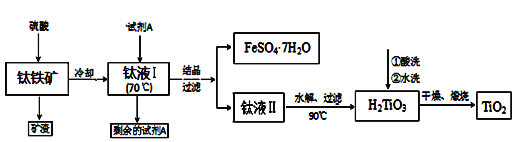
已知有关反应包括:
酸溶FeTiO3(s)+2H2SO4(aq)→FeSO4(aq)+TiOSO4(aq)+2H2O(l)
水解TiOSO4(aq)+2H2O(l)→H2TiO3(s)+H2SO4(aq)
(1)试剂A为____,钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品收率降低,原因____;
(2)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现红色,说明H2TiO3中存在的杂质离子是__________。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2会略发黄,发黄的杂质是_____________(填化学式)。
方法2:
Ⅰ.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4;
II.将SiCl4分离,得到纯净的TiCl4;
III.在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O,洗涤和干燥;
IV.TiO2·xH2O高温分解得到TiO2。
(1)TiCl4水解生成TiO2x H2O的化学方程式为____________________;
(2)检验TiO2x H2O中Cl-是否被除净的方法是____________________;金属钛被称为“21世纪金属”,工业制备金属钛是在800~900℃及惰性气体的保护下,在密闭反应器中,将TiCl4以一定的流速通入熔化的镁即可。主要涉及以下反应:
①TiO2+2Cl2+C→TiCl4+CO2
②TiCl4+2Mg → 2MgCl2+Ti
(3)下列推断不合理的是________
A.钛在高温下可能易与氧气反应
B.镁的熔点比钛的熔点高
C.钛的金属活动性比镁的金属活动性强
D.反应②产生的MgCl2可作为电解法制取镁的原料
(4)请完成以TiO2、Cl2和焦炭为原料制取金属Ti和Mg的流程图,并用箭头标明物料循环。___________________
【答案】铁粉 由于TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO4·7H2O中导致TiO2产率降低 Fe2+ Fe2O3 TiCl4+(2+x)H2O![]() TiO2xH2O↓+4HCl 取少量水洗液,滴加硝酸酸化AgNO3溶液,若不产生白色沉淀,说明Cl-已除净 BC
TiO2xH2O↓+4HCl 取少量水洗液,滴加硝酸酸化AgNO3溶液,若不产生白色沉淀,说明Cl-已除净 BC 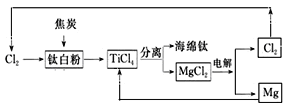
【解析】
含有Fe2O3、SiO2的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)加硫酸,在90℃温度下,溶解,过滤,滤液中含有FeSO4(aq)、TiOSO4(aq)和Fe2(SO4)3(aq),加铁粉(试剂A),把三价铁离子还原为亚铁离子,降温到70℃,结晶过滤,得到硫酸亚铁晶体,滤液为TiOSO4(aq),滤液温度升高到90℃,使TiOSO4水解生成H2TiO3固体,洗涤、干燥、煅烧得到TiO2。
(1)由流程可知Fe2(SO4)3与Fe粉反应产生FeSO4(aq),试剂A应为铁粉;由题中信息可知,TiOSO4容易水解,升高温度促进水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO47H2O中导致TiO2产率降低;
(2)取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,说明没有Fe3+,再加H2O2后出现红色,说明有Fe3+,则原来含有Fe2+,加H2O2后Fe2+被氧化为Fe3+;H2TiO3中的二价铁易被氧化为三价铁,煅烧时会生成Fe2O3,TiO2含有少量的Fe2O3会呈现黄色;
(1)设TiCl4的系数为1,根据元素守恒,TiO2xH2O的系数为1,HCl的系数为4;再根据O元素守恒,可知H2O的系数为(2+x),方程式为TiCl4+(2+x)H2O![]() TiO2xH2O↓+4HCl;
TiO2xH2O↓+4HCl;
(2)沉淀吸附溶液中的Cl-,根据发生反应:Cl-+Ag+=AgCl↓,可知检验TiO2x H2O中Cl-是否被除净的方法是:取最后一次的少量洗涤液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净;
(3)A. 工业制备金属钛是在800~900℃及惰性气体的保护下,说明钛在高温下可能易与氧气反应生成二氧化钛,A正确;
B. 镁易熔化熔点较低,镁的熔点比钛的熔点低,故B错误;
C. 活泼性强的金属能置换活泼性弱的金属,Mg能置换Ti,说明Mg比Ti活泼,C错误;
D. 电解熔融的MgCl2能制取镁,所以反应②产生的MgCl2可作为电解法制取镁的原料,故D正确;
故合理选项是BC;
(4)TiO2、Cl2和焦炭在高温条件下生成TiCl4和CO2,再用Mg单质置换TiCl4得到Ti和MgCl2,电解熔融的氯化镁又能得到Mg和Cl2,则以TiO2、Cl2和焦炭为原料制取金属Ti和Mg的流程图为: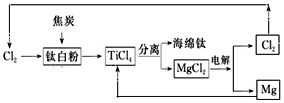 。
。


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
【题目】25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) ![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )

A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
C. 25 ℃时,该反应的平衡常数K=2.2
D. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用Pt电极电解1 L浓度均为0.1 mol·L-1的HCl、CuSO4的混合溶液,装置如图,下列说法正确的是( )
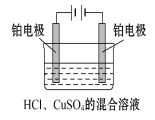
A.电解开始时阴极有H2放出
B.电解开始时阳极上发生:Cu2++2e-Cu
C.整个电解过程中,SO42-不参与电极反应
D.当电路中通过电子的量超过0.1 mol时,此时阴极放电的离子发生了变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。
②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。
图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列表述中正确的是
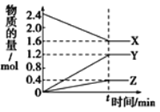
A. 反应的化学方程式为2X=3Y+Z
B. 若t=4,则0~t的X的化学反应速率为0.1mol·L-1·min-1
C. t时,正、逆反应都不再继续进行,反应达到平衡状态
D. 温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体的体积分数φ(CO2)随时间t变化的曲线如图所示。下列说法正确的是( )
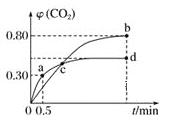
A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:Kb>Kd
D.0→a点时,0到0.5 min反应速率v(CO)=0.3 molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,其分子中各原子的原子半径大小关系为______,碳原子核外有___种运动状态不同的电子。
(2)氰化钠(NaCN)中,N元素显-3价,则非金属性N___________C(填“<”、“=”或“>”),写出氰化钠的电子式_______________。
(3)氰化钠属于剧毒物质,可用双氧水或硫代硫酸钠处理。
(a)用双氧水处理,发生的反应为:NaCN+H2O2+H2O→A+NH3↑,则A的化学式为___。
(b)NaCN与Na2S2O3二者等物质的量反应可得到两种含硫元素的离子,其中一种遇到Fe3+显血红色。写出该反应的离子方程式____________。
(4)NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是______;恰好反应后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com