
分析 设出H2O(g)和O2的物质的量,根据关系式2Na2O2~O2、2NaHCO3~H2O计算过氧化钠和碳酸氢钠的物质的量即可.
解答 解:排出气体只含H2O(g)和O2且物质的量相等,设H2O(g)和O2的物质的量都是xmol,
根据关系式2Na2O2~O2可知,原混合物中Na2O2的物质的量为2xmol,
根据H元素守恒可知NaHCO3的物质的量为:n(NaHCO3)=2n(H2O)=2xmol,
原固体混合物中m:n=2xmol:2xmol=1:1,
故答案为:1:1.
点评 本题考查化学方程式的计算,题目难度不大,明确发生的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:解答题
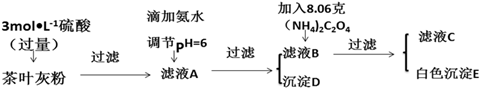
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 4.1 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Fe2+、I-、Cl-三种离子一定存在 | |
| B. | CO32-一定不存在,不能确定Na+和Cl-是否存在 | |
| C. | Fe3+与Fe2+至少有一种 | |
| D. | 该溶液中c(Cl-)至少为0.2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100g质量分数为98%的浓硫酸中所含有的氧原子数为4NA | |
| B. | 足量的Fe与6.72LCl2反应转移的电子数为0.6NA | |
| C. | 密闭容器中1molN2与4molH2反应生成的NH3分子数小于2NA | |
| D. | 3g乙烷含有共用电子对为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1mol•L-1氨水中加几滴酚酞,再加等体积的醋酸铵溶液,观察红色是否变浅 | |
| B. | 测定0.1 mol•L-1NH4C1溶液的酸碱性 | |
| C. | 测定0.lmol•L-1氨水的pH | |
| D. | 比较浓度均为0.1 mol•L -1的氨水与NaOH溶液的导电能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥⑦ | B. | ③④⑥⑦ | C. | ①②⑤⑧ | D. | ①③⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:

 ,
, +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaCl.
+NaCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、甲苯、乙醇、乙酸都可以发生取代反应 | |
| B. | 可用浓溴水来区分乙醇和苯酚 | |
| C. | 乙酸乙酯在无机酸或碱存在时都能发生水解反应 | |
| D. | 能发生水解反应的有机物只有卤代烃和酯类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将纯水加热的过程中,KW变大,酸性增强 | |
| B. | 保存FeSO4溶液时,加入稀HNO3抑制Fe2+水解 | |
| C. | NaHCO3溶液蒸干、灼烧至恒重,最终得到NaHCO3固体 | |
| D. | 相同浓度的下列溶液中:①CH3COONH4、②CH3COONa、③CH3COOH中,c(CH3COCO-)由大到小的顺序是②>①>③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com