
����Ŀ����ͼ1��ϸ����3�ֻ����ﺬ��������ͼ��ͼ2�ǻ�ϸ����Ԫ�غ���������ͼ��������������ȷ���ǣ�������
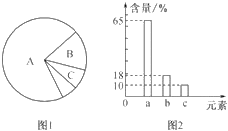
A. ͼ2����������Ԫ����̼Ԫ�أ�����ϸ���к������Ļ������й�
B. ��ͼ1��ʾ����ϸ������B��������ж����ԣ���غ���Ԫ��ΪC��H��O��N
C. ��ͼ1��ʾ����ϸ������A��B�����ﹲ�е�Ԫ���к���������ͼ2�е�a
D. ��ͼ1��ʾϸ�������л����ﺬ��������ͼ���� A�������к�������Ԫ��Ϊͼ2�е�b
���𰸡�A
��������
��ͼʾ����ɿ�֪��ͼ1��A��B��C�ֱ���ˮ�������ʺ�֬�ʣ�ͼ2��a��b��c�ֱ�����Ԫ�ء�̼Ԫ�غ���Ԫ����
���ϸ����ˮ������࣬����������Ԫ������Ԫ�أ�A������ͼ1��ʾ����ϸ������B�������ǵ����ʣ����ж����ԣ���غ���Ԫ��ΪC��H��O��N��B��ȷ����ͼ1��ʾ����ϸ������Aˮ��B�����ʻ����ﹲ�е�Ԫ���к���������ͼ2�е�a��Ԫ�أ�C��ȷ����ͼ1��ʾϸ�������л����ﺬ��������ͼ���� A�����ﵰ�����к�������Ԫ��Ϊͼ2�е�b̼Ԫ�أ�D��ȷ����ˣ������ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ� ��
A.��״���£�22.4LH2O�����ķ�����ΪNA
B.14g���������ĵ�ԭ����ΪNA
C.��״���£�22.4LNH3�����ĵ�����ΪNA
D.1molNa��Cl2��Ӧת�Ƶ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100��ʱ����0.100mol N2O4�������1L���ݳ�յ��ܱ������У�������Ӧ��N2O4��g��![]() 2NO2��g������һ��ʱ��Ը����������ʵ�Ũ�Ƚ��з����õ�������ݡ��ش��й�����;
2NO2��g������һ��ʱ��Ը����������ʵ�Ũ�Ƚ��з����õ�������ݡ��ش��й�����;
ʱ��(s) | 0 | 20 | 40 | 60 | 80 |
c(N2O4)/mol��L��1 | 0.100 | c1 | 0.050 | c3 | c4 |
c(NO2)/mol��L��1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
��c3________c4(�>������<������)��
�������������£��ӷ�Ӧ��ʼֱ���ﵽ��ѧƽ��ʱ��N2O4��ƽ����Ӧ����Ϊ_________mol��L��1��s��1��
�۴�ƽ������������ĸı��ʹNO2����Ũ���������_______(�����)��
A�������������ݻ� B���ٳ���һ������N2O4
C�������һ������NO2 D���ٳ���һ������He
��������ͬ�����£���ʼʱֻ����0.200 mol NO2���壬��ﵽƽ��ʱNO2�����ת����Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������绯��ʴʱ�������Ϸ����ķ�Ӧ�ǣ� ��
A.2H++2e-=H2��B.2H2O+O2+4e-=4OH-
C.Fe-2e-=Fe2+D.4OH--4e-=O2��+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧһѡ��5���л���ѧ������ij�������Ա�Ϊ��Ҫԭ�ϣ���ȡ����·�ߺϳ�����ҩ���������ӡ�
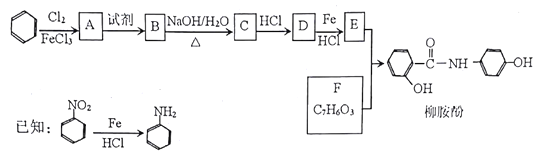
�ش��������⣺
(1)F�Ļ�ѧ����____����E��F���������ӵķ�Ӧ������____��
(2)д����A����B��Ӧ������Լ�_____��
(3)д����B����C�Ļ�ѧ����ʽ____��
(4)���������ӣ�����˵����ȷ����____��
a���ɷ���ˮ�ⷴӦ b��������������Ӧ
c��1 mol�����������Ժ�2molNaOH��Ӧ d�������巢��ȡ����Ӧ
(5)д������ͬʱ��������������F��ͬ���칹��Ľṹ��ʽ_________��
�ٱ�������2�ֲ�ͬ��ѧ��������ԭ�ӣ����ܷ���������Ӧ��������FeCl3������ɫ��Ӧ
(6)4-��������������(![]() )����Ҫ�ľ�ϸ�����м��壬д���ɱ�����(
)����Ҫ�ľ�ϸ�����м��壬д���ɱ�����(![]() )�������Ʊ�4-���������������ĺϳ�·��_______________�����Լ����ܼ���ѡ�����ϳ�·�ߵ���д��ʽ��������ʾ������ͼ��
)�������Ʊ�4-���������������ĺϳ�·��_______________�����Լ����ܼ���ѡ�����ϳ�·�ߵ���д��ʽ��������ʾ������ͼ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���һ���������ܺ�����������Һ��Ӧ����( )
A.�Ҵ�B.��֬C.����D.��ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����˵�����й����е�����ת����ʽ��
(1)���ˮ��_________
(2)���ε�صķŵ���̡�_________
(3)ú����Ϊȼ��ȼ�ա�________
(4)ֲ��Ĺ�����á�_________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���鷨�벻���ķ��ı�(�ʡ�ī��ֽ����)�������õ��Ǻ�����ī�õ�ī���Լ���ֽ(����ֽ)������̨�õ���ʯ����Ҫ�ɷ�������
A. ���ǡ�̿�ڡ������ʡ�����
B. ���ϡ�ú̿�����ǡ�����
C. �����ʡ�̿�ڡ����ǡ�����
D. �����ʡ�ú̿�����ǡ��л�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���10mL 0.2mol��L��l����(H2C2O4)��Һ����μ����Ũ�ȵ�NaOH��Һ���й��������ʵ���������Һ��pH������ͼ��ϵ������˵����ȷ����

A. HC2O4������Һ��ˮ��̶ȴ��ڵ���̶�
B. ��V (NaOH) =10 mLʱ��Һ�д��ڣ�c(HC2O4��)+c(C2O42��)+c(H2C2O4)=0.1mol��L��l
C. ��V (NaOH) =15mLʱ����Һ�д��ڣ�c(Na+)>c(HC2O4��)>c(C2O42��)>c (OH��)>c(H+��
D. ��V (NaOH) =20 mLʱ����Һ�д�����c(OH��) =c (HC2O4��)+c (H2C2O4)+c(H+)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com