
【题目】CoP、FeS2、NiS2等物质对电化学氢析出反应有良好的催化活性和稳定性。请回答下列问题:
(1)基态Co原子价层电子的电子排布图(轨道表达式)为________________,基态P原子的电子占据最高能级的电子云轮廓图为_______。
(2)PH3的沸点_____(填“高于”或“低于”)NH3,原因是______________。
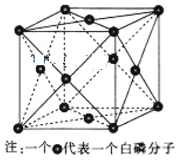
(3)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加德罗常数的数值为NA,其晶体密度的计算表达式为______g·cm-3。
【答案】![]() 哑铃形或纺锤形 低于 NH3分子之间形成氢键,PH3分子之间为范德华力,氢键比范德华力更强,故NH3的沸点比PH3的高
哑铃形或纺锤形 低于 NH3分子之间形成氢键,PH3分子之间为范德华力,氢键比范德华力更强,故NH3的沸点比PH3的高 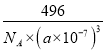
【解析】
(1)Co是27号元素,处于第四周期第VIII族,价电子排布式为3d74s2,结合泡利原理、洪特规则画出价电子排布图;基态P原子的电子占据最高能级为3p能级;
(2)分子间形成氢键会使其熔沸点升高;
(3)均摊法计算晶胞中P4的数目,计算晶胞质量,晶体密度=晶胞质量÷晶胞体积。
(1)Co是27号元素,处于第四周期第VIII族,价电子排布式为3d74s2,结合泡利原理、洪特规则,价电子排布图为![]() ;基态P原子的电子占据最高能级为3p能级,电子云形状为哑铃形;
;基态P原子的电子占据最高能级为3p能级,电子云形状为哑铃形;
(2)NH3分子之间形成氢键,PH3分子之间为范德华力,氢键比范德华力更强,故NH3的沸点比PH3的高;
(3)晶胞中P4的数目=8×![]() +6×
+6×![]() =4,晶胞质量=4×
=4,晶胞质量=4×![]() g,晶体密度=4×
g,晶体密度=4×![]() g÷(a×10-7 cm)3=
g÷(a×10-7 cm)3=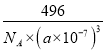 gcm-3。
gcm-3。


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:高中化学 来源: 题型:
【题目】用混有硫酸亚铁和硫酸镁等杂质的锰矿(含MnO2、MnCO3)生产硫酸锰,实验室模拟生产过程如下:
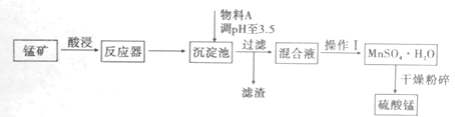
已知金属离子完全沉淀时的pH值如下:Fe3+:3.5;Fe2+:9.5;Mn2+:10.8;Mg2+:11.6。
(1)反应器中发生氧化还原反应的离子方程式是________。
(2)从经济效益考虑,物料A可以是________。
(3)硫酸锰和硫酸镁的溶解度曲线如右图所示:
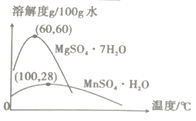
则操作Ⅰ包含的主要操作为________。
(4)MnSO4·H2O在1150℃条件下分解,产物是Mn2O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示式错误的是( )
A. Na+的轨道表示式:![]() B. Na+的结构示意图:
B. Na+的结构示意图:![]()
C. Na的电子排布式:1s22s22p63s1 D. Na的外围电子排布式:3s1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组通过如图所示的流程来制取少量亚硝酸钠晶体(NaNO2),并对其进行纯度测定和相关性质的实验。
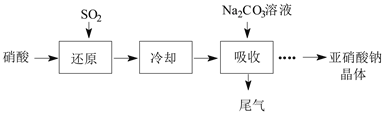
已知:Ⅰ.Na2CO3+NO+NO2=2NaNO2+CO2;Na2CO3+2NO2=NaNO2+NaNO3+CO2
Ⅱ.NaNO2是白色固体,易被氧化。
(1)“还原”步骤中被还原的元素是___(填元素符号)。此时SO2从底部通入,硝酸从顶部以雾状喷下,其目的是___。
(2)若使“吸收”步骤中NOX完全转化为NaNO2,则理论上“还原”步骤中SO2与HNO3的物质的量之比为___。
(3)该课外兴趣小组对实验制取的NaNO2晶体进行纯度测定:
a.称取2.000g样品,将其配成250mL溶液。
b.先向锥形瓶内加入40.00mL0.100mol·L-1的H2SO4溶液,加热至40~50℃。冷却后再向其中加入20.00mL0.100mol·L-1KMnO4溶液,充分混合。
c.最后用待测的样品溶液与之恰好完全反应,重复三次,平均消耗样品溶液50.00mL。(NaNO2与KMnO4反应的关系式为:2KMnO4~5NaNO2)
①整个测定过程中应迅速操作,不宜耗时过长,否则样品的纯度___(“偏大”、“偏小”或“无影响”),原因是___。
②通过计算,该样品中NaNO2的质量分数是___,可能含有的杂质有___(写出其中一种即可)。
(4)该课外兴趣小组将NaNO2溶液逐滴加入到含淀粉KI的酸性溶液中,溶液变蓝,同时放出NO气体,该反应的离子方程式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2+O2![]() 2SO3在密闭容器中进行。下列说法正确的是( )
2SO3在密闭容器中进行。下列说法正确的是( )
A.使用催化剂不能改变反应速率
B.达平衡时SO2与SO3的浓度相等
C.增大压强能加快反应速率
D.SO2与O2反应能完全转化为SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温时,向2L密闭容器中通入一定量的气体X和Y,发生反应:3X(g)+Y(g)![]() 2Z(g) ΔH>0。Y的物质的量n(Y)随时间t变化的曲线如图所示。下列说法正确的是( )
2Z(g) ΔH>0。Y的物质的量n(Y)随时间t变化的曲线如图所示。下列说法正确的是( )
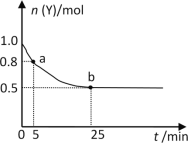
A.该反应为放热反应
B.0~5min内,以X表示的化学反应速率是0.02mol·L-1·min-1
C.b点时该反应达到了最大限度,反应停止
D.25min时,c(Z)=0.5mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含铬化合物有毒,对人畜危害很大。因此含铬废水必须进行处理才能排放。已知:Cr3+![]() Cr(OH)3
Cr(OH)3![]() CrO2-。
CrO2-。
(1)在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
①写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式_______________________。
②用离子方程式表示溶液pH不能超过10的原因__________________________________。
③若处理后的废水中残留的c(Fe3+)=2×10-13 mol/L,则残留的Cr3+的浓度为___________。(已知:Ksp[Fe(OH)3]=4.0×10-38 Ksp[Cr(OH)3]=6.0×10-31)
(2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合成氢氧化物沉淀而除去。
①写出阴极的电极反应式__________________________。
②电解法中加入氯化钠的作用是______________________。
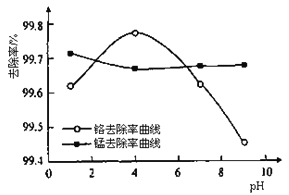
(3)某化学兴趣小组以含+6价铬和+2价锰的工业废水为试样,研究铁屑用量和pH对废水中铬、锰去除率的影响。
①取100mL废水于250 mL三角瓶中,调节pH到规定值,分别加入不同量的废铁屑.得到铁屑用量对铬和锰去除率的影响如下图所示。则在pH一定时,废水中铁屑用量为____________时,锰、铬去除率最好。
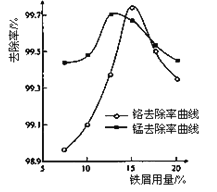
②取100mL废水于250 mL三角瓶中,加入规定量铁粉,调成不同的pH。得到pH对铬和锰去除率的影响如下图所示。则在铁屑用量一定时,废水pH=__________时锰、铬去除率最好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.请将下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法),并指出是属于化学变化还是物理变化。
①溶解 ②裂解 ③分馏 ④裂化 ⑤干馏 ⑥蒸馏 ⑦电解 ⑧过滤 ⑨萃取
(1)把煤转化为焦炉气、煤焦油和焦炭等_______、_________变化。
(2)从原油中分离出汽油、煤油、柴油等__________、__________变化。
(3)将重油转化为汽油_____________、__________变化。
(4)将海水淡化_______、_____变化。
Ⅱ.在鸡蛋清溶液中加入以下各物质时:
(1)加入大量饱和硫酸铵,产生絮状沉淀,此过程叫做蛋白质的________________。
(2)加入浸制动物标本时用的福尔马林溶液(主要成分为甲醛),产生絮状沉淀此过程称为蛋白质的______。
(3)加入浓硝酸并微热,现象为________,这是由于浓硝酸与蛋白质发生了____________反应的缘故。
(4)乙醇(CH3CH2OH)在铜做催化剂时与氧气反应的方程式________________。
(5)制备聚乙烯的化学方程式________________________________________________。
(6)制备一氯乙烷的方程式_____________________________________________。
(7)制备1,2—二氯乙烷的方程式___________________________________________。
Ⅲ.①花生油中所含人体所需的主要营养物质为________(填“糖类”、“油脂”或“蛋白质”)。
②吃饭时,咀嚼米饭一会儿后感觉有甜味,是因为淀粉发生了____________(填字母)反应。
A.分解 B.水解 C.裂解
(2)在日常生活中,下列做法错误的是________。
A.用燃烧法鉴别毛织品和棉织品
B.用纯碱洗涤锅盖上的油渍
C.用闻气味的方法鉴别白酒和米醋
D.用淀粉溶液鉴别加碘食盐和不含碘的食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过测定混合气中O2含量可计算已变质的Na2O2 (含Na2CO3) 纯度,实验装置如图(Q为弹性良好的气囊)。下列分析错误的是
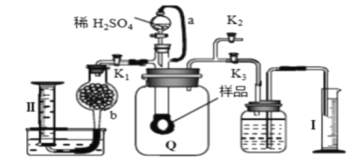
A. 干燥管b中装入碱石灰
B. Q气球中产生的气体主要成份O2、CO2
C. 测定气体总体积必须关闭K1、K2,打开K3
D. 读完气体总体积后,关闭K3,缓缓打开K1;可观察到Q气球慢慢缩小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com