
【题目】钼(Mo)是一种难熔稀有金属,我国的钼储量居世界前列,钼及其合金在冶金、环保和航天等方面有着广泛的应用。
(1)Mo可被发烟硝酸及氢氟酸氧化生成X和Y(少量),X和Y中Mo价态相同,硝酸本身被还原为NO2,该反应中氧化剂与还原剂的物质的量之比为6:1,则Mo在氧化产物中的化合价为___________;
(2)已知:2Mo(s)+3O2(g)===2MoO3(s) △H1;
MoS2(s)+2O2(g)===Mo(s)+2SO2(g) △H2。
写出MoS2(s)与氧气反应生成MoO3(s)的热化学方程式_____________________________;
(3)碳酸钠作固硫剂并用氢还原辉钼矿的原理为
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO (g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO (g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
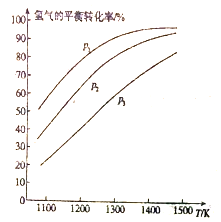
(a)不同压强下温度与H2平衡转化率的关系

(b)0.1MPa下温度与平衡时气体成分的关系
①由图(a)可知,该反应△H___________0(填“>”或“<”),p1、p2、p3由大到小的顺序为___________;
②由图(b)可知,B点时H2的平衡转化率为___________;
③A点对应的平衡常数K=___________(MPa)2。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)电氧化法提纯钼的原理:将辉钼矿(MoS2)放入装有食盐水的电解槽中,用惰性电极电解,MoS2被氧化为MoO42-和SO42-。
①辉钼矿应放入电解槽的___________(填“阴极区”或“阳极区”);
②阴极的电极反应式为_________________________________。
【答案】+6 2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g) △H=△H1+2△H2 > p1<p2<p3 66.7% 4×10-4 阳极区 2H2O+2e-=H2↑+2OH-
【解析】
(1)根据电子守恒确定Mo在氧化产物中的化合价;
(2) ①2Mo(s)+3O2(g)═2MoO3(s)△H1,②MoS2(s)+2O2(g)═Mo(s)+2SO2(g)△H2,根据盖斯定律可知,②×2+①得到2MoS2(s)+7O2(g)═2MoO3(s)+4SO2(g);
(3)①升高温度平衡向吸热反应方向移动,增大压强平衡向气体总物质的量减小的方向移动;
②由图(b)可知,B点时H2的体积分数为25%,设起始时氢气的物质的量为1mol,此时氢气的转化率为α,则:
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO (g)+4H2O(g)+2Na2S(s)
Mo(s)+2CO (g)+4H2O(g)+2Na2S(s)
起始物质的量(mol) 1 0 0
变化物质的量(mol) α 0.5α α
平衡物质的量(mol) 1-α 0.50α α
![]() =25%,即可解得α;
=25%,即可解得α;
③图1中A点氢气和水蒸气的体积分数相等,均为40%,而由反应方程式可知一氧化碳的体积分数为水蒸气的一半,即为20%,说明氢气、一氧化碳和水蒸气的物质的量之比为2:1:2,由此根据表达式求Kp;
(4)电解池的阳极发生氧化反应,阴极发生还原反应,并结合MoS2被氧化为MoO42-和SO42-分析解题。
(1)Mo可被发烟硝酸及氢氟酸氧化生成X和Y(少量),X和Y中Mo价态相同,设Mo在氧化产物中的化合价为x价,则Mo元素从0价升高为x价,而硝酸本身被还原为NO2,氮元素从+5价降为+4价,在该反应中氧化剂与还原剂的物质的量之比为6:1,根据电子守恒可知:6×(5-4)=1×(x-0),解得:x=+6,即Mo在氧化产物中的化合价为+6;
(2)已知①2Mo(s)+3O2(g)═2MoO3(s)△H1,②MoS2(s)+2O2(g)═Mo(s)+2SO2(g)△H2,由盖斯定律计算②×2+①得:2MoS2(s)+7O2(g)═2MoO3(s)+4SO2(g)△H=△H1+2△H2;
(3) ①升高温度平衡向吸热反应方向移动,由图像(a)可知升高温度,氢气的转化率增大,说明平衡正向移动,正方向为吸热反应,即该反应△H>0;增大压强平衡向气体总物质的量减小的方向移动,对MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO (g)+4H2O(g)+2Na2S(s)可知,增大平衡逆向移动,氢气的转化率降低,则由图像(a)可知p1<p2<p3;
Mo(s)+2CO (g)+4H2O(g)+2Na2S(s)可知,增大平衡逆向移动,氢气的转化率降低,则由图像(a)可知p1<p2<p3;
②由图(b)可知,B点时H2的体积分数为25%,设起始时氢气的物质的量为1mol,此时氢气的转化率为α,则:
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO (g)+4H2O(g)+2Na2S(s)
Mo(s)+2CO (g)+4H2O(g)+2Na2S(s)
起始物质的量(mol) 1 0 0
变化物质的量(mol) α 0.5α α
平衡物质的量(mol) 1-α 0.50α α
![]() =25%,解得:α=66.7%,即B点时H2的平衡转化率为66.7%;
=25%,解得:α=66.7%,即B点时H2的平衡转化率为66.7%;
③图1中A点氢气和水蒸气的体积分数相等,均为40%,而由反应方程式可知一氧化碳的体积分数为水蒸气的一半,即为20%,说明氢气、一氧化碳和水蒸气的物质的量之比为2:1:2,Kp=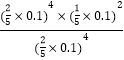 =4×10-4,;
=4×10-4,;
(4)电氧化法提纯钼的原理:将辉钼矿(MoS2)放入装有食盐水的电解槽中,用性电极电解,
①用惰性电极电解时,阳极发生氧化反应,则MoS2被氧化为MoO42-和SO42-,辉钼矿应放入电解槽的阳极区;
②电解池的阴极发生还原反应,则阴极的电极反应式为2H2O+2e-=H2↑+2OH-。


科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A.共价化合物中可能含离子键
B.离子化合物中可能含共价键
C.非金属原子间不可能形成离子键
D.非极性键只存在于双原子单质分子里
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 60gSiO2和12g金刚石中各含有4NA个Si-O键和4NA个C-C键
B. H2O(g)通过足量Na2O2(s)充分反应,固体增重bg时,反应中转移的电子数为bNA/2
C. 1L0.2mo1/ LNaHCO3溶液中含HCO3-和CO32-的离子数之和为0.2NA
D. 足量的Mg与稀H2SO4完全反应,生成2.24LH2时,转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某草酸二酯结构简式如图,下列说法正确的是
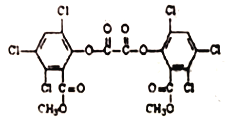
A. 草酸二酯的分子式为C26H22Cl6O8
B. 1mol草酸二酯与氢氧化钠稀溶液反应时(苯环上卤素不水解),最多消耗4molNaOH
C. 草酸二酯能发生的反应类型有氧化、还原、取代、加成、聚合、酯化
D. 草酸二酯酸性条件下充分水解可以得到三种有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化锌是有机合成中重要催化剂,无水氯化锌为白色粉末,易潮解,沸点为732℃。久置市售氯化锌常含Zn(OH)Cl,影响催化效果。实验室用HC1气体“置换”除水、升华氯化锌相结合的方法提纯市售氯化锌。
(1)选用下图所示的装置(可以重复选用)进行实验,装置接口依次连接的合理顺序为:a→___________。
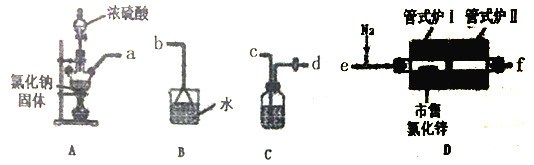
(2)装置A盛氯化钠固体的仪器名称是___________,装置C中试剂是___________。
(3)实验开始时,通入HC1和N2,将管式炉I,Ⅱ升温至150℃,装置D中发生的化学反应方程式为___________;此时通入N2的目的是______________________;
(4)反应一段时间后保持管式炉I、Ⅱ温度为350℃,保证将水除尽,再______________________;(填操作)最后在氮气保护下将氯化锌刮出玻璃管外,保存待用。
(5)若称取100.00g市售氯化锌样品,经提纯最终得到高纯氯化锌100.3g,则样品中氯化锌纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语,说法正确的是( )
①2N ②Mg2+ ③![]() ④H2 ⑤
④H2 ⑤![]()
A. ①表示两个氮分子B. ②与⑤均表示镁离子
C. ③表示一氧化碳中碳元素的化合价为+2D. ④表示2个氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消細,与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
(1)方法一的离子方程式为______________________________。
(2)方法二中被氧化的物质是_______,若反应中有0.1 mol电子转移,则产生的ClO2气体在标准状况下的体积为_________L。
(3)用双线桥法标出方法一中方程式电子转移的方向和数目_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温密闭容器中发生反应:CaCO3(s)![]() CaO(s)+CO2(g) H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是
CaO(s)+CO2(g) H>0,反应达到平衡后,tl时缩小容器体积, x随时间(t)变化的关系如下图所示。x不可能是

A. υ逆(逆反应速率) B. ρ(容器内气体密度)
C. m(容器内CaO质量) D. Qc(浓度商)
查看答案和解析>>
科目:高中化学 来源: 题型:
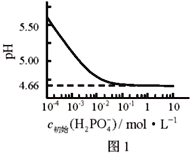
【题目】LiH2PO4是制备电池的重要原料。室温下,LiH2PO4溶液的pH随c初始(H2PO4–)的变化如图1所示,H3PO4溶液中H2PO4–的分布分数![]() 随pH的变化如图2所示,
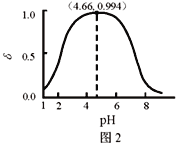
随pH的变化如图2所示,![]() 下列有关LiH2PO4溶液的叙述正确的是
下列有关LiH2PO4溶液的叙述正确的是
A. 含P元素的粒子有H2PO4–、HPO42–、PO43–
B. LiH2PO4溶液中存在2个平衡
C. 用浓度大于1 mol·L-1的H3PO4溶液溶解Li2CO3,当pH达到4.66时,H3PO4几乎全部转化为LiH2PO4
D. 随c初始(H2PO4–)增大,溶液的pH明显变小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com