
ЁОЬтФПЁПФГЮоЩЋШмвКжаКЌгаMg2+ЁЂAl3+ЁЂFe3+ЁЂCu2+ЁЂNH4+ЁЂNa+жаЕФвЛжжЛђМИжжЃЌШЁ100mLИУШмвКЃЌЯђЦфжаВЛЖЯЕЮМгNaOHШмвКЃЌВњЩњЕФГСЕэЫцзХNaOHЬхЛ§БфЛЏЕФЙиЯЕШчЭМЫљЪОЃЌ дђЯТСаа№ЪіВЛе§ШЗЕФЪЧ

A. ИУШмвКжавЛЖЈВЛКЌFe3+ЁЂCu2+
B. ИУШмвКжавЛЖЈКЌгаMg2+ЁЂAl3+ЁЂNH4+ЃЌЧвШ§епЮяжЪЕФСПХЈЖШжЎБШЮЊ1ЁУ1ЁУ1
C. ЫљМгNaOHШмвКЮяжЪЕФСПХЈЖШЮЊ1mol/L
D. aЕуЕНbЕуЃЌУЛгаЗЂЩњЛЏбЇЗДгІ
ЁОД№АИЁПD
ЁОНтЮіЁПМгШыNaOHШмвККѓЃЌСЂМДЩњГЩГСЕэЃЌaЕуЕНbЕуЃЌГСЕэЕФЮяжЪЕФСПВЛБфЃЌЫЕУїШмвКжавЛЖЈДцдкNH4+ЃЌЫцКѓГСЕэж№НЅМѕЩйжСВЛБфЃЌЫЕУїКЌгаMg2+ЁЂAl3+ЁЃAЁЂИУШмвКЮоЩЋЃЌЫЕУїШмвКжавЛЖЈВЛКЌFe3+ЁЂCu2+ЃЌбЁЯюAе§ШЗЃЛBЁЂИљОнЩЯЪіЗжЮіЃЌИУШмвКжавЛЖЈКЌгаMg2+ЁЂAl3+ЁЂNH4+ЃЌИљОнЭМЯёЃЌЧтбѕЛЏУОКЭЧтбѕЛЏТСИї0.01molЃЌяЇИљРызгЯћКФ10mL1mol/LЧтбѕЛЏФЦШмвКЃЌЫЕУїяЇИљРызгЕФЮяжЪЕФСПЮЊ0.01molЃЌвђДЫШ§жжРызгЕФЮяжЪЕФСПХЈЖШжЎБШЮЊ1ЃК1ЃК1ЃЌбЁЯюBе§ШЗЃЛ CЁЂИљОнЭМЯёЃЌШмНт0.01molЧтбѕЛЏТСашвЊ0.01molЧтбѕЛЏФЦЃЌЫљМгNaOHШмвКЮяжЪЕФСПХЈЖШ=![]() =1mol/LЃЌбЁЯюCе§ШЗЃЛDЁЂaЕуЕНbЕуЃЌГСЕэЕФЮяжЪЕФСПВЛБфЃЌЗЂЩњяЇИљРызггыЧтбѕИљРызгЕФЗДгІЃЌЫЕУїШмвКжавЛЖЈДцдкNH4+ЃЌ бЁЯюDДэЮѓЁЃД№АИбЁDЁЃ
=1mol/LЃЌбЁЯюCе§ШЗЃЛDЁЂaЕуЕНbЕуЃЌГСЕэЕФЮяжЪЕФСПВЛБфЃЌЗЂЩњяЇИљРызггыЧтбѕИљРызгЕФЗДгІЃЌЫЕУїШмвКжавЛЖЈДцдкNH4+ЃЌ бЁЯюDДэЮѓЁЃД№АИбЁDЁЃ


 зДдЊЗЛШЋГЬЭЛЦЦЕМСЗВтЯЕСаД№АИ
зДдЊЗЛШЋГЬЭЛЦЦЕМСЗВтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪГЃЮТЯТГЪвКЬЌЕФЪЧ ЃЈ ЃЉ
A.МзЭщB.ввЯЉC.ввШВD.БН
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛИіШнЛ§ЙЬЖЈЕФУмБеШнЦїжаЃЌЗЂЩњЗДгІЃКCO(g)ЃЋ2H2(g)![]() CH3OH(g)ЁЁІЄH<0ЁЃЕк2 minЪБжЛИФБфвЛИіЬѕМўЃЌЗДгІЧщПіШчЯТБэЃК
CH3OH(g)ЁЁІЄH<0ЁЃЕк2 minЪБжЛИФБфвЛИіЬѕМўЃЌЗДгІЧщПіШчЯТБэЃК
ЪБМф | c(CO)/mol/L | c(H2)/mol/L | c(CH3OH)/mol/L |
Ц№ЪМ | 1 | 3 | 0 |
Ек2 min | 0.8 | 2.6 | 0.2 |
Ек4 min | 0.4 | 1.8 | 0.6 |
Ек6 min | 0.4 | 1.8 | 0.6 |
ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ(ЁЁЁЁ)
A. Ек4 minжСЕк6 minИУЛЏбЇЗДгІДІгкЦНКтзДЬЌ
B. Ек2 minЪБЃЌШчЙћжЛИФБфФГвЛЬѕМўЃЌдђИФБфЕФЬѕМўПЩФмЪЧНЕЕЭЮТЖШ
C. Ек2 minЪБЃЌШчЙћжЛИФБфФГвЛЬѕМўЃЌдђИФБфЕФЬѕМўПЩФмЪЧЪЙгУДпЛЏМС
D. Ек6 minЪБЃЌЦфЫћЬѕМўВЛБфЃЌШчЙћЩ§ИпЮТЖШЃЌе§ЗДгІЫйТЪдіДѓ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉНЋЕШЬхЛ§ЕШЮяжЪЕФСПХЈЖШЕФДзЫсКЭЧтбѕЛЏФЦШмвКЛьКЯКѓЃЌШмвКГЪ_______ЃЈЬюЁАЫсадЁБЃЌЁАжаадЁБЛђЁАМюадЁБЃЌЯТЭЌЃЉЃЛpHЃН3ЕФДзЫсКЭpHЃН11ЕФЧтбѕЛЏФЦШмвКЕШЬхЛ§ЛьКЯКѓШмвКГЪ__________ЁЃ
ЃЈ2ЃЉГЃЮТЪБЃЌгаpHЃН12ЕФNaOHШмвК20mLЃЌвЊЪЙЫќЕФpHБфЮЊ11ЁЃЃЈЛьКЯЙ§ГЬжаЬхЛ§БфЛЏКіТдВЛМЦЃЉШчЙћМгШыеєСѓЫЎЃЌгІМг_________mLЃЛШчЙћМгШыpHЃН10ЕФNaOHШмвКЃЌгІМг__________mLЁЃ
ЃЈ3ЃЉдк25 ЁцЪБЃЌгаpHЮЊxЕФбЮЫсКЭpHЮЊyЕФNaOHШмвКЃЌШЁVx LИУбЮЫсЭЌИУNaOHШмвКжаКЭЃЌашVy L NaOHЃЌЧѓЃК
ЂйШєx+y=14ЪБЃЌдђVx/Vy=_______________(ЬюЪ§жЕ)ЁЃ
ЂкШєx+y=13ЪБЃЌдђVx/Vy=_______________(ЬюЪ§жЕ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПТШЛЏЕт(ICl)ЕФЛЏбЇаджЪИњТШЦјЯрЫЦЃЌдЄМЦЫќИњЫЎЗДгІЕФзюГѕЩњГЩЮяЪЧ
AЃЎHClКЭHIO BЃЎHIКЭHClO CЃЎHClO3КЭHIO DЃЎHClOКЭHIO
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌМзЁЂввЁЂБћЁЂЖЁЫФжжЦјЬЌЬўЕФЗжзгжаЫљКЌЕчзгЪ§ЗжБ№ЮЊ10ЁЂ14ЁЂ16ЁЂ18ЃЌЯТСаЙигкетЫФжжЦјЬЌЬўЕФЭЦЖЯе§ШЗЕФЪЧ
A. ЫФжжЦјЬЌЬўжажСЩйгаСНжжЛЅЮЊЭЌЗжвьЙЙЬх
B. ПЩвдгУЫсадИпУЬЫсМиШмвКМјБ№ввКЭБћ
C. БћЗжзгжаЫљгадзгОљдкЭЌвЛЦНУцЩЯ
D. ввКЭЖЁЪєгкЭЌЯЕЮя
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзЁЂввСНжжЛЏКЯЮяЖМжЛКЌгаXЁЂYСНжждЊЫиЃЌМзЁЂввжаXдЊЫиЕФжЪСПЗжЪ§ЗжБ№ЮЊ30.4КЭ25.9%ЃЌШєвбжЊМзЕФЗжзгЪНЪЧXY2ЃЌдђввЕФЗжзгЪНжЛПЩФмЪЧ(ЁЁЁЁ)
AЃЎXY BЃЎX2Y CЃЎX2Y3 DЃЎX2Y5
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЁЂYЁЂZЁЂMЁЂNЮхжжГЃМћЖЬжмЦкдЊЫидзгАыОЖЫцдзгађЪ§БфЛЏШчЭМЁЃвбжЊXЕФвЛжждзгЕФжЪСПЪ§ЮЊ18ЃЌжазгЪ§ЮЊ10ЃЛYКЭNeдзгЕФКЫЭтЕчзгЪ§ЯрВю1ЃЛMЕФЕЅжЪЪЧвЛжжГЃМћЕФАыЕМЬхВФСЯЃЛNЕФдзгАыОЖдкЭЌжмЦкжїзхдЊЫижазюаЁЃЛYЁЂZЁЂNШ§жждЊЫиЕФзюИпбѕЛЏЮяЖдгІЫЎЛЏЮяСНСНжЎМфПЩЗЂЩњЗДгІЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧ
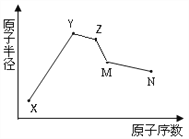
A. NЁЂZСНжждЊЫиЕФРызгАыОЖЯрБШЧАепНЯаЁ
B. MЁЂNСНжждЊЫиЕФЦјЬЌЧтЛЏЮяЕФЮШЖЈадЯрБШКѓепНЯЧП
C. XгыYСНжждЊЫизщГЩЕФвЛжжЛЏКЯЮяжавѕЁЂбєРызгЕФИіЪ§БШЮЊ1:1
D. ЙЄвЕЩЯгУЕчНтYКЭNаЮГЩЕФЛЏКЯЮяЕФШлШкЬЌжЦШЁYЕФЕЅжЪ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЬюПе
ЃЈ1ЃЉЯТСадзгЃК ![]() CЁЂ
CЁЂ ![]() NЁЂ
NЁЂ ![]() NaЁЂ
NaЁЂ ![]() HЁЂ
HЁЂ ![]() UЁЂ
UЁЂ ![]() KЁЂ
KЁЂ ![]() UжаЙВгажждЊЫиЃЌжжКЫЫиЃЌЛЅЮЊЭЌЮЛЫиЃЎ
UжаЙВгажждЊЫиЃЌжжКЫЫиЃЌЛЅЮЊЭЌЮЛЫиЃЎ
ЃЈ2ЃЉвѕРызгЕФжазгЪ§ЮЊNЃКAXnЉЙВгаxИіЕчзгЃЌдђN= ЃЎ
ЃЈ3ЃЉгаЯТСаЮяжЪжаNH3ЁЂNa2OЃЌCO2ЁЂCaCl2ЁЂCCl4ЁЂH2O2ЁЂN2ЁЂNaHCO3ЁЂNaOHЃЌNa2O2ЁЂNH4ClЪєгкКЌЗЧМЋадМќЕФРызгЛЏКЯЮяЕФЪЧ
ЃЈ4ЃЉЯТСаЧњЯпЗжБ№БэЪОдЊЫиЕФФГжжаджЪгыКЫЕчКЩЪ§ЕФЙиЯЕЃЈXЮЊКЫЕчКЩЪ§ЃЌYЮЊдЊЫиЕФгаЙиаджЪЃЉЃЎАбгыЯТУцдЊЫигаЙиЕФаджЪЯрЗћЕФЧњЯпБъКХЬюШыЯргІЕФПеИёжаЃК 
ЂйЕкЂђAзхдЊЫиЕФзюЭтВуЕчзгЪ§ЃЛ
ЂкЕкШ§жмЦкдЊЫиЕФзюИпЛЏКЯМлЃЛ
ЂлМюН№ЪєЕЅжЪЕФШлЕу ЃЎ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com