
【题目】在反应3Cl2+2FeBr2=2FeCl3+2Br2中得到电子的元素是( )
A.Fe
B.Fe和Cl
C.Cl
D.Br
科目:高中化学 来源: 题型:
【题目】(1)键线式![]() 表示的分子式____________________;名称是________________________。
表示的分子式____________________;名称是________________________。
(2)  中含有的官能团的名称为_____________________________________。
中含有的官能团的名称为_____________________________________。
(3)丙基的两种结构简式为____________________、______________________。
(4)写出下列有机物的结构简式
2,2,3,3-四甲基戊烷_____________________________
3,4-二甲基-4-乙基庚烷______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某溶液逐滴加入氢氧化铁胶体中,开始时产生沉淀,继续滴加时沉淀又溶解,则该溶液是( )
A.2mol·L-1氯化钾溶液
B.2mol·L-1酒精溶液
C.2mol·L-1蔗糖溶液
D.2mol·L-1硝酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废气中的含氮氧化物是主要的大气污染物,因此脱出废气中的含氮氧化物对于保护大气环境具有重要的意义。
(1)汽车的大量使用是城市大气中含氮氧化物的主要来源。
①汽车燃油中一般不含有氮元素,汽车尾气中的NO是如何产生的?___________(用化学方程式表示)。
②NO易被O2氧化为NO2。其他条件不变时,NO的氧化率[α(NO)%]与温度、压强的关系如图所示。则p1________p2(填“>”、“<”或“=”);温度高于800℃时,α(NO)几乎为0的原因是_____。
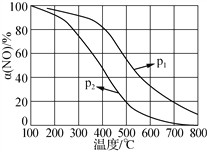
(2)利用氨气脱除NO是大气污染防治研究的热点,过程中涉及的反应为:
主反应:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
副反应:
①4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-905.5kJ/mol
4NO(g)+6H2O(g) ΔH=-905.5kJ/mol
②4NH3(g)+4O2(g)![]() 2N2O(g)+6H2O(g) ΔH=-1104.9kJ/mol
2N2O(g)+6H2O(g) ΔH=-1104.9kJ/mol
③4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ΔH=-1269.0kJ/mol
2N2(g)+6H2O(g) ΔH=-1269.0kJ/mol
回答下列问题:
主反应的ΔH为____________________;保持其它条件相同,使用两种不同的催化剂,主反应NO的转化率与温度关系如图所示,选用催化剂I的优势有_________________(写出一点即可);R点对应的温度为210℃,低于210℃,NO的转化率是不是对应温度下的平衡转化率,请作出判断并写出理由__________________。
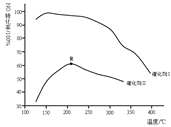
(3)碱液吸收法:用Na2CO3溶液吸收NO2生成CO2.若每4.6gNO2和Na2CO3溶液反应时转移电子数为0.05mol,则反应的离子方程式是__________。
(4)常温下,在通入O2的条件下用0.1mol/L的NaOH溶液吸收NO,产物为NaNO3 和NaNO2。已知反应后溶液的pH=12,溶液中NO2-浓度为5.6×10-2mol/L(忽略反应过程中溶液体积变化,HNO2的电离平衡常数Ka=5.1×10-4),则:
①![]() =________mol/L
=________mol/L
②反应后溶液中NO3-的浓度约为___________mol/L
③某溶液中c(NO2-)=1.0×10-6mol/L,取该溶液5mL,加入一滴0.1mol/L硝酸银溶液(一滴为0.05mL),通过计算说明能否产生沉淀______________。(Ksp(AgNO2)=2×10-8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证Na2CO3固体中是否含有NaHCO3,下列实验事实及判断中,正确的是 ( )
A.溶于水后加石灰水,看有无沉淀B.加稀盐酸观察是否有气体产生
C.加热后称重,看质量是否变化D.在无色火焰上灼烧,观察火焰是否呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂的组成可用“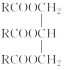 ”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同。分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1—CH=CH—R2
”来表示,其中R为碳原子数目多于10的链烃基,可以相同也可以不同。分子式为C51H92O6的某油脂在稀硫酸中加热水解后得到A、B两种物质,若A的相对分子质量为92(已知:R1—CH=CH—R2![]() R1—COOH+R2—COOH),则:
R1—COOH+R2—COOH),则:
(1)B的分子式为________,A的结构简式为________。
(2)B![]() C+D,等物质的量的C、D分别与足量的NaOH溶液反应时,消耗的NaOH的质量之比为1∶2,C、D的相对分子质量相差30且C、D结构中均无支链,则B的结构简式为________。
C+D,等物质的量的C、D分别与足量的NaOH溶液反应时,消耗的NaOH的质量之比为1∶2,C、D的相对分子质量相差30且C、D结构中均无支链,则B的结构简式为________。
(3)若A和乙酸在一定条件下反应后生成相对分子质量为134的E,写出E所有可能的结构简:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为短周期元素①~⑧的部分性质,下列说法正确的是
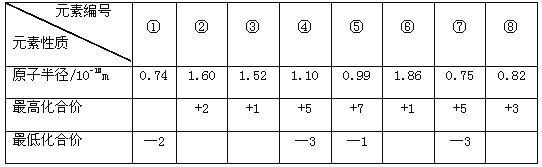
A. 元素⑦的气态氢化物稳定性比元素④的气态氢化物稳定性强
B. 元素④的最高价氧化物对应水化物的酸性比元素⑤的最高价氧化物对应水化物的酸性强
C. 元素①⑧形成的化合物具有两性
D. 上表8种元素中,元素③的最高价氧化物对应水化物的碱性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠电池由于其快速充放电的特性受到科研工作者的重视,某钠离子钛基电池电池结构如图所示,电解质为含钠离子的高聚物,已知电池的反应方程式为2NaxCn+xNaTi2(PO4)3![]() 2nC+ xNa3Ti2(PO4)3。下列关于该电池说法正确的是
2nC+ xNa3Ti2(PO4)3。下列关于该电池说法正确的是
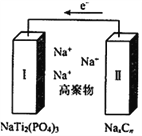
A. 放电时电池正极为NaxCn B. 放电时Na+向电极Ⅱ移动
C. 充电时阳极反应:NaxCn-xe-=nC+xNa+ D. 充电时电极Ⅰ与外电源正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中将2molNaHCO3(s)和一定量Na2O2混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,反应后固体的物质的量(n)的取值范围是( )
A. n≥1 B. 1<n<2 C. 2≤n<4 D. n≥4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com