
【题目】化合物M是一种二苯乙炔类液晶材料,其分子结构与最简单的二苯乙炔类液晶材料![]() 相似。以两种苯的同系物A、G为原料合成M的一种路线如图(部分反应条件略去):
相似。以两种苯的同系物A、G为原料合成M的一种路线如图(部分反应条件略去):
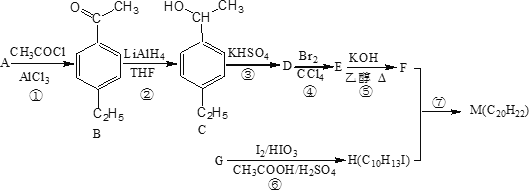
回答下列问题;
(1)A的分子式为___。
(2)推测在B转化为C的反应中LiAlH4/THF的作用是___。
(3)D的分子式为C10H12,①~⑦中属于消去反应的是___。
(4)写出⑤的化学方程式:___。
(5)满足下列条件的B的同分异构体有___种。
Ⅰ.能发生银镜反应;
Ⅱ.分子中苯环上只有两种化学环境不同的氢原子。
(6)H分子为对位二取代苯结构,其核磁共振氢谱共有三组峰,且峰面积之比为9:2:2。写出H和M的结构简式:H___,M___。
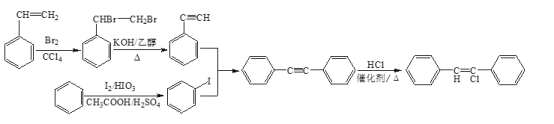
(7)参照上述合成路线,设计一条以苯和苯乙烯为原料制备![]() 的合成路线___。(其它无机试剂任选)
的合成路线___。(其它无机试剂任选)
合成路线流程示例:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
【答案】C8H10 还原剂 ③⑤ 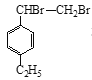 +2KOH
+2KOH +2KBr+2H2O 11种
+2KBr+2H2O 11种 ![]()
![]()
【解析】
A为苯的同系物,A经过反应后生成B,B的结构为 ,由其结构推测,A为乙苯,A生成B发生的是取代反应;由B生成C,显然发生的是还原反应,生成的C(
,由其结构推测,A为乙苯,A生成B发生的是取代反应;由B生成C,显然发生的是还原反应,生成的C( )的结构中含有能发生消去反应的醇羟基;D的分子式为C10H12,C的分子式为C10H14O,因此,可知C生成D发生的应是消去反应,D的结构为
)的结构中含有能发生消去反应的醇羟基;D的分子式为C10H12,C的分子式为C10H14O,因此,可知C生成D发生的应是消去反应,D的结构为 ;那么由D生成E,发生的是加成反应,结果是在分子内引入卤素原子;由E生成F的条件推测,发生的是消去反应,那么F的结构为
;那么由D生成E,发生的是加成反应,结果是在分子内引入卤素原子;由E生成F的条件推测,发生的是消去反应,那么F的结构为 。H的分子式为C10H13I,由题可知,其分子中含有3类等效氢原子,并且个数分别为9,2,2;考虑到H为苯环的二取代物,所以H的结构只能为
。H的分子式为C10H13I,由题可知,其分子中含有3类等效氢原子,并且个数分别为9,2,2;考虑到H为苯环的二取代物,所以H的结构只能为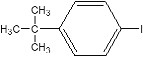 ;G为苯的同系物,所以G的结构为
;G为苯的同系物,所以G的结构为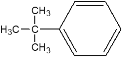 ;H与F反应后生成M,分子式为C20H22,并且其结构与二苯乙炔相似,所以M的结构为
;H与F反应后生成M,分子式为C20H22,并且其结构与二苯乙炔相似,所以M的结构为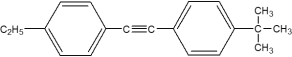 ,那么H与F发生的则是取代反应。
,那么H与F发生的则是取代反应。
(1)通过分析可知,A为乙苯,分子式为C8H10;
(2)通过分析可知,B生成C发生的是还原反应,所以LiAlH4/THF的作用是还原剂;
(3)通过分析可知,①至⑦中,属于消去反应的有③⑤;
(4)通过分析可知,反应⑤是消去反应,方程式为: +2KOH
+2KOH![]()
 +2KBr+2H2O;
+2KBr+2H2O;
(5)B的结构为 ,那么若其同分异构体含有苯环,并且能发生银镜反应,则一定含有醛基,且除苯环和醛基外,其余均为饱和结构;为了保证其同分异构体的苯环上有两种氢原子,所以至少苯环上要有两个取代基,并且取代基对位排列,这两个取代基可能为-CHO和CH3CH2CH2-或-CHO和(CH3)2CH-或-CH2CHO和CH3CH2-或-CH2CH2CHO和-CH3或
,那么若其同分异构体含有苯环,并且能发生银镜反应,则一定含有醛基,且除苯环和醛基外,其余均为饱和结构;为了保证其同分异构体的苯环上有两种氢原子,所以至少苯环上要有两个取代基,并且取代基对位排列,这两个取代基可能为-CHO和CH3CH2CH2-或-CHO和(CH3)2CH-或-CH2CHO和CH3CH2-或-CH2CH2CHO和-CH3或![]() 和CH3-,共计5种结构;若苯环上有3个取代基,符合条件的结构为/span>
和CH3-,共计5种结构;若苯环上有3个取代基,符合条件的结构为/span>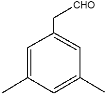 和
和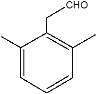 2种结构;若苯环上有4个取代基,这四个取代基只能是3个甲基和一个醛基,符合要求的结构有
2种结构;若苯环上有4个取代基,这四个取代基只能是3个甲基和一个醛基,符合要求的结构有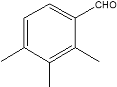 ,
,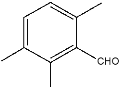 ,
,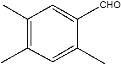 ,
,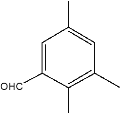 ,共计4种结构;综上所述,符合要求的B的同分异构体共计5+2+4=11种结构;
,共计4种结构;综上所述,符合要求的B的同分异构体共计5+2+4=11种结构;
(6)通过分析可知,H的结构为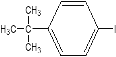 ,M的结构为
,M的结构为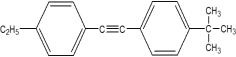 ;
;
(7)由![]() 的结构可知,可由
的结构可知,可由 和HCl加成得到,而获得
和HCl加成得到,而获得 可由苯乙炔与碘苯按照反应⑦生成;因此合成路线为:
可由苯乙炔与碘苯按照反应⑦生成;因此合成路线为: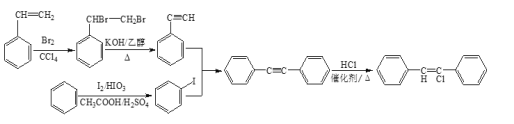 。
。


科目:高中化学 来源: 题型:
【题目】密闭容器中进行如下反应:X(g)+3Y(g)![]() 2Z(g),X、Y、Z起始浓度分别是0.2mo1/L、0.6mol/L、0.4mol/L,当达到平衡时,下列数据可能正确的是
2Z(g),X、Y、Z起始浓度分别是0.2mo1/L、0.6mol/L、0.4mol/L,当达到平衡时,下列数据可能正确的是
A. X为0.25mol/L,Z为0.5mol/L B. Y为1.2mo1/L
C. X为0.3mol/L,Z为0.3mol/L D. Z为0.6mo1/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一种特殊的热激活电池示意图,当无水LiCl-KCl混合物受热熔融后即可工作。该电池总反应为:PbSO4(s)+2LiCl+Ca(s) = CaCl2(s)+Li2SO4+Pb(s)。下列说法不正确的是( )
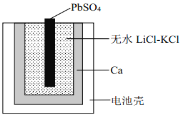
A.PbSO4电极发生还原反应
B.负极的电极反应:Ca + 2Cl--2e-=CaCl2
C.用LiCl和KCl水溶液代替无水LiCl-KCl,可将该电池改为常温使用的电池
D.放电时 Li+、 K+向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是①NO和NO2,②NO2和O2,③NO和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体体积分别为V1、V2、V3,则下列关系正确的是( )
A.V1>V2>V3B.V1>V3>V2
C.V2>V3>V1D.V3>V1>V2
查看答案和解析>>
科目:高中化学 来源: 题型:
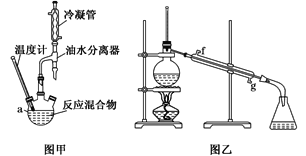
【题目】丙烯酸甲酯是一种重要的化工原料,实验室制备丙烯酸甲酯的反应、装置示意图和有关数据如下:
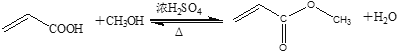
沸点(℃) | 溶解性 | 毒性 | |
丙烯酸 | 142 | 与水互溶,易溶于有机溶剂 | 有毒 |
甲醇 | 65 | 与水互溶,易溶于有机溶剂 | 有毒 |
丙烯酸甲酯 | 80.5 | 难溶于水,易溶于有机溶剂 | 无毒 |
实验步骤:
①向三颈瓶中加入10.0g丙烯酸、6.0g甲醇、数滴浓硫酸和几粒沸石,缓慢加热。
②反应30min后,停止加热,反应液冷却后,分别用少量水、饱和碳酸氢钠溶液和水洗涤。
③取上层油状液体,用少量无水MgSO4干燥后蒸馏,收集70~90℃馏分。
回答下列问题:
(1)反应过程采用水浴加热,原因是___。
(2)图甲中油水分离器的作用是___。
(3)判断酯化反应达到平衡的现象为__。
(4)第一次水洗的主要目的是___。
(5)在洗涤、分液步骤中用到的主要玻璃仪器有烧杯、___。
(6)图乙所示装置中冷却水的进口为___(填字母)。
为分析产率,进行如下实验:将收集到的馏分平均分成五份,取出一份置于锥形瓶中,加入2.5mol/LKOH溶液10.00mL,加热使之完全水解;用酚酞作指示剂,向冷却后的溶液中滴加0.5mol/LHCl溶液,中和过量的KOH,共消耗盐酸20.00mL。
(7)本次制备实验的产率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊接性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。
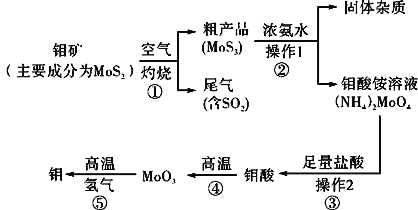
(1)反应①的尾气可以再利用,写出应用该尾气制得的两种重要化学试剂:___。
(2)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有:___。
(3)钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶液生成钼酸钠;三氧化钼不溶于盐酸或稀硫酸。钼酸钠的化学式为___。
(4)工业上制备还原性气体CO和H2的反应原理为CO2+CH4![]() 2CO+2H2,CH4+H2O
2CO+2H2,CH4+H2O![]() CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为___。
CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,互为同分异构体的是 ( )
A. 与
与
B. 与CH3CH2CH2CH2Cl
与CH3CH2CH2CH2Cl
C.CH4与CH3CH3
D.CH3CH(CH3)CH2CH2CH3与CH3CH2CH2CH(CH3)CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图:![]() 。下列有关说法不正确的是
。下列有关说法不正确的是
A.分子式为C3H4O3B.分子中σ键与π键个数之比为3:1
C.分子中既有极性键也有非极性键D.分子中碳原子的杂化方式全部为sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、NH![]() 、Mg2+、Al3+、Fe3+、CO
、Mg2+、Al3+、Fe3+、CO![]() 、SO
、SO![]() 、NO
、NO![]() 中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法不正确的是( )
中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法不正确的是( )
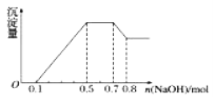
A.溶液中一定含有NH![]() B.溶液中一定含有Al3+
B.溶液中一定含有Al3+
C.溶液中一定含有NO![]() D.溶液中一定含有SO
D.溶液中一定含有SO![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com