
| A、正极发生还原反应 |
| B、通入CH4的电极为负极 |
| C、该电池使用一段时间后应补充KOH |
| D、燃料电池工作时,溶液中的OH-向正极移动 |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
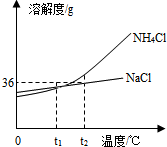 如图是氯化铵和氯化钠两种固体物质的溶解度曲线,下列叙述错误的是( )
如图是氯化铵和氯化钠两种固体物质的溶解度曲线,下列叙述错误的是( )| A、t2℃时,向18g NaCl固体加入50g水,充分搅拌后固体能全部溶解 |
| B、0℃时,NaCl和NH4C1两种物质的饱和溶液都升温至t1℃,两种溶液中溶质的质量分数相等 |
| C、t2℃时,将NH4Cl溶液降温到0℃,不一定有晶体析出 |
| D、NH4Cl中含有少量NaCl,可以用冷却热饱和溶液的方法提纯NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a>b>c |
| B、b>c>a |
| C、a=b=c |
| D、a=b<c |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.8 g?mol-1 |
| B、11.6 g?mol-1 |
| C、23.2 g?mol-1 |
| D、46.4 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱电解质化学式 | CH3COOH | HCN | H2CO3 | NH3.H2O |
| 电离平衡常数 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7K2=5.6×l0-11 | 1.8×l0-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、③④ | C、①③ | D、②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com