
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
| B、碳酸氢钠溶液与过量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、硫酸亚铁溶液中加入酸化的双氧水:Fe2++2H++H2O2=Fe3++2H2O |
| D、向明矾溶液中滴加过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、0.9%氯化钠溶液 |
| B、0.9%氯化铵溶液 |
| C、1.25%碳酸氢钠溶液 |
| D、5%葡萄糖溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、+184.6kJ?mol-1 |
| B、+92.3kJ?mol-1 |
| C、-184.6kJ?mol-1 |
| D、-92.3kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol CH4含有的电子数为NA |
| B、标准状况下,2.24L的CCl4中含有的氯原子数为0.4NA |
| C、常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数为0.4NA |
| D、标准状况下,2.24L的乙炔含碳原子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、84消毒液和洁厕灵混合使用会产生有毒气体:Cl-+ClO-+2H+=Cl2↑+H2O |
| B、向水玻璃中加入盐酸有白色沉淀生成:2H++SiO32-=H2SiO3↓ |
| C、SO2使紫色石蕊溶液变红色:SO2+H2O?2H++SO42- |
| D、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3C1O-+3H2O=Fe(OH)3↓+3HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热聚丙烯废塑料得到的产物如下表:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
| ① |
| ② |
| ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
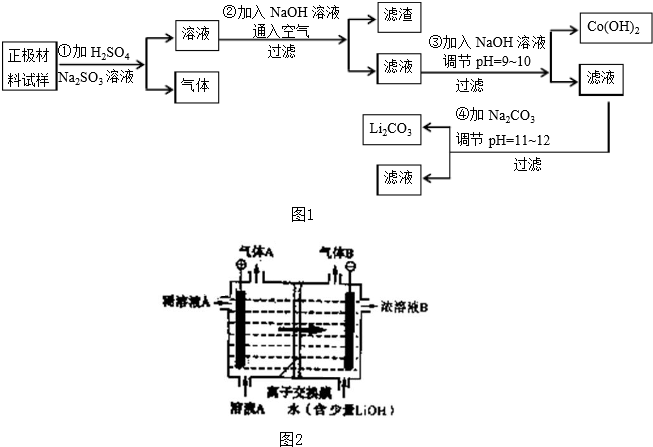
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com