
| ʵ����� | ʵ������ | ʵ���� |
| 1 | ����AgNO3��Һ | �а�ɫ�������� |
| 2 | ��������NaOH��Һ������ | �ռ�������0.896L������ɱ�״���� |
| 3 | ��������BaCl2��Һ�������ó���ϴ�ӡ�������أ���������м�������ϡ���ᣬϴ�ӡ�������� | ��һ�γ��ض���Ϊ6.27g���ڶ��γ��ض���Ϊ2.33g |
���� ��̼���������������Ȼ������ǰ�ɫ���������ʵ��1��ȷ���Ƿ��������Ӳ���ȷ��������ʵ��2��֪��������ӣ�����ʵ��3��֪����һ����̼�ᱵ�����ᱵ������Һ��һ������CO32-��SO42-������Һ��һ������Ba2+��Mg2+��
ʵ��2�м�����NaOH��Һ�����ȣ����ռ������壬�������Ϊ�����������ݱ���°�����������Լ���笠������ʵ�����
ʵ��3��̼�ᱵ���������ᣬ���ᱵ���������ᣬ��˼��������ʣ��2.33g����ΪBaSO4��������̼�غ㼴���������Һ��c��SO42-������CO32-�������ʵ���Ũ�ȣ�
������Ϸ����Լ����и��������ݿ�֪����Һ�п϶����ڵ�������NH4+��CO32-��SO42-�������㣬NH4+�����ʵ���Ϊ0.04 mol��CO32-��SO42-�����ʵ����ֱ�Ϊ0.02 mol��0.01 mol�����ݵ���غ��K+һ�����ڣ��Դ������
��� �⣺��1��̼���������������Ȼ������ǰ�ɫ���������ʵ��1�õ�������ȷ�����Ȼ�������ʵ��1��Cl-�Ƿ���ڵ��ж��ǣ��ʴ�Ϊ����
��2����ʵ���֪��Һ��һ�����е�������ΪCO32-��SO42-����̼�ᱵ���������ᣬ���ᱵ�������������֪���������ʣ��2.33g����ΪBaSO4���������غ��֪��Һ��c��SO42-��=$\frac{\frac{2.33g}{233g/mol}}{0.1L}$=0.1mol/L��6.27g������̼�ᱵ������Ϊ6.27g-2.33g=3.94g������̼�غ��֪��Һ��c��CO32-��=$\frac{\frac{3.94g}{197g/mol}}{0.1L}$=0.2mol/L��NH4+�����ʵ���Ϊ$\frac{0.896L}{22.4L/mol}$=0.04 mol��c��NH4+��=$\frac{0.04mol}{0.1L}$=0.4mol/L����Һ�п϶����ڵ�������NH4+��CO32-��SO42-���ɵ���غ��֪����֪c��K+����0.1mol/L��2+0.2mol/L��2-0.4mol/L��1=0.2mol/L����֪��Һ��һ������K+��
�ʴ�Ϊ��c��SO42-��=0.1mol/L��c��CO32-��=0.2mol/L��c��NH4+��=0.4mol/L��c��K+����0.2mol/L��
���� ���⿼�����ӵļ��飬Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�ӦΪ���Ĺؼ������ط�����ʵ�顢���������Ŀ��飬ע�����غ��Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
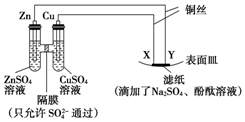
| A�� | XΪ����������������Ӧ | B�� | Y����ֽ�Ӵ������������� | ||
| C�� | XΪ����������������Ӧ | D�� | X����ֽ�Ӵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
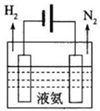 ���ڻ������������䡢�����⡱��ȼú�������������������;�dz��㷺��
���ڻ������������䡢�����⡱��ȼú�������������������;�dz��㷺��| ���ۼ� | H-H | N-H | N=N |
| ����/kJ•mol-1 | 436 | 390.8 | 946 |
| NH3��������17%�İ�ˮ | ��ˮ NH4HSO3 | |
| �۸�Ԫ/kg�� | 1.0 | 1.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ�к���1mol Na2SO4 | B�� | 1mol Na2SO4����1Lˮ�� | ||
| C�� | ��Һ��c��Na+��=2 mol•L-1 | D�� | 1L��Һ�к���2molNa+��2mol SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ��� | �¶�/�� | H2SO4���/mL | KI��Һ���/mL | H2O���/mL | ������Һ /mL | ������ɫʱ��/s |
| A | 40 | 10 | 5 | 5 | 1 | 5 |
| B | TB | 10 | 5 | 5 | 1 | û������ɫ |
| C | 5 | 10 | 5 | 5 | 1 | 39 |
| D | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 450mL | B�� | 500mL | C�� | 400mL | D�� | ����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ���� | C�� | ԭ���� | D�� | ��ԭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��K�Ľṹ��ʽΪ
��K�Ľṹ��ʽΪ ��
��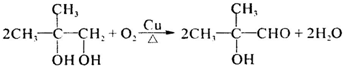 ��
�� $��_{��}^{ŨH_{2}SO_{4}}$
$��_{��}^{ŨH_{2}SO_{4}}$ +H2O��
+H2O���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com