
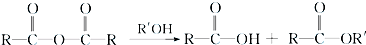
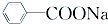 +RCl→
+RCl→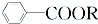 +NaCl;
+NaCl; .
. .
.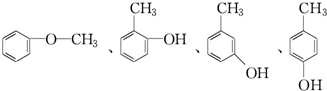 .
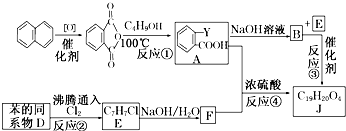
.分析 D为苯的同系物,D与氯气反应生成E,结合E的分子式可知,D为 ,E与NaOH的水溶液发生取代反应生成F,F与浓溴水混合不产生白色沉淀,则E为
,E与NaOH的水溶液发生取代反应生成F,F与浓溴水混合不产生白色沉淀,则E为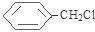 ,F为
,F为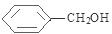 .根据信息I可知反应①为取代反应,则A的结构简式为
.根据信息I可知反应①为取代反应,则A的结构简式为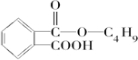 ;反应④为酯化反应,J为为
;反应④为酯化反应,J为为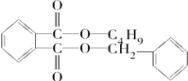 ,控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应生成B,B与E(
,控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应生成B,B与E( )发生反应生成J(
)发生反应生成J( ),则B为
),则B为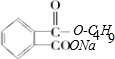 .
.
解答 解:D为苯的同系物,D与氯气反应生成E,结合E的分子式可知,D为 ,E与NaOH的水溶液发生取代反应生成F,F与浓溴水混合不产生白色沉淀,则E为
,E与NaOH的水溶液发生取代反应生成F,F与浓溴水混合不产生白色沉淀,则E为 ,F为
,F为 .根据信息I可知反应①为取代反应,则A的结构简式为
.根据信息I可知反应①为取代反应,则A的结构简式为 ;反应④为酯化反应,J为为
;反应④为酯化反应,J为为 ,控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应生成B,B与E(
,控制反应条件,使物质A中的支链Y不与NaOH溶液发生反应生成B,B与E( )发生反应生成J(
)发生反应生成J( ),则B为
),则B为 .
.
(1)根据分析可知,E为 ,含有的官能团为氯原子,F的结构简式为:
,含有的官能团为氯原子,F的结构简式为: ,F中官能团为-OH,羟基的电子式为
,F中官能团为-OH,羟基的电子式为 ,
,
故答案为:氯原子; ;
;
(2)A+F→J的化学方程式:的化学反应方程式是: ,
,
故答案为: ;
;
(3)反应①属于取代反应,反应④属于取代反应,
故答案为:取代反应;取代反应;
(4)F( )的属于芳香烃衍生物的同分异构体的结构简式:
)的属于芳香烃衍生物的同分异构体的结构简式: ,
,
故答案为: ;
;
(5)C4H9OH的同分异构体中属于醇类,可以看作丁烷中H原子被-OH取代,正丁烷被取代形成2种醇,异丁烷被取代形成2种醇,故有4种,其中具有手性碳原子的同分异构体的结构简式为:CH3CH2CH(OH)CH3,
故答案为:4;CH3CH2CH(OH)CH3.
点评 本题考查有机的推断与合成,注意根据转化中有机物结构特点进行推断,熟练掌握官能团的结构与性质,注意对题目信息的应用,是对有机化学基础的综合考查,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,K+、Ca2+、Cl2、Br -可以大量共存 | |
| B. | 与足量Ca( OH)2溶液反应的离子方程式:Ca2++OH-+HS03═CaS03↓+H20 | |
| C. | 与FeCI3溶液反应的离子方程式:SO32-+2 Fe3++H20═SO42-+2Fe2++2H+ | |
| D. | 能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
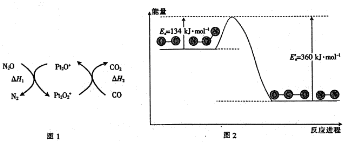
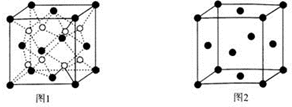
| A. | 由图1可知:△H1=△H+△H2 | |
| B. | 由图2可知△H=-226 kJ/mol | |
| C. | 为了实现转化需不断向反应器中补充Pt2O+和Pt2O2+ | |
| D. | 由图2可知该反应正反应的活化能大于逆反应的活化能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
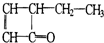 ,可表示为
,可表示为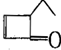 ,某有机物
,某有机物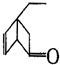 的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )
的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 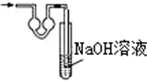 | B. | 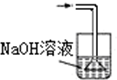 | C. | 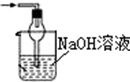 | D. | 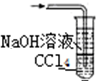 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通常元素的化合价与其原子的质量数有密切的关系 | |
| B. | 已知铱的一种核素是${\;}_{77}^{191}$Ir,则其核内的中子数是114 | |
| C. | ${\;}_{6}^{14}$C和${\;}_{7}^{17}$N的质量数相同,但质子数不同,所以互称为同位素 | |
| D. | 钾的原子结构示意图为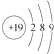 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:6 | B. | 6:1 | C. | 1:5 | D. | 1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com