
| A£® | 0.8 | B£® | 1.3 | C£® | 3.1 | D£® | 0.32 |
·ÖĪö øł¾Ż¼×ĶéŗĶCO”¢H2µÄČ¼ÉÕČČ²¢½įŗĻ¹ÜµĄĆŗĘųµÄÖĘ·ØæÉÖŖ¹ÜµĄĆŗĘųÖŠCOŗĶH2µÄ±ČĄżĄ“½ųŠŠ¼ĘĖć£®
½ā“š ½ā£ŗÓÉÉś²śĖ®ĆŗĘųµÄ·“Ó¦æÉÖŖ£¬ĆŗĘųÖŠCOÓėH2Ģå»ż±ČĪŖ1£ŗ1£®ÉčČ¼ÉյĹܵĄĆŗĘųŗĶĢģČ»ĘųµÄĪļÖŹµÄĮæ¾łĪŖ4mol£¬ŌņČ¼ÉÕ4molĆŗĘų·ÅČČ£ŗQ1=571.6KJ+566kJ=1137.6KJ£¬¶ųČ¼ÉÕ4molĢģČ»Ęų·ÅČČQ2=4”Į890.3 kJ=3561.2KJ£¬ŗóÕߏĒĒ°ÕßµÄ$\frac{4”Į890.3KJ}{£Ø571.6+566£©KJ}$=$\frac{3561.2KJ}{1137.6KJ}$”Ö3.1±¶£¬
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖ·“Ó¦·Å³öČČĮæµÄ¼ĘĖć£¬½āĢā¹Ų¼üŹĒøł¾ŻĆŗĘųµÄÖĘ·ØæÉÖŖĆŗĘųÖŠCOÓėH2Ģå»ż±ČĪŖ1£ŗ1£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
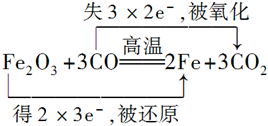 £®
£®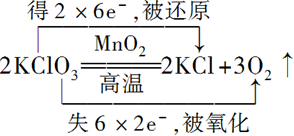 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.3 mol/L Na2SO4ČÜŅŗÖŠŗ¬ÓŠNa+ŗĶSO42-×ÜĪļÖŹµÄĮæĪŖ0.9mol | |
| B£® | µ±1LĖ®ĪüŹÕ22.4LNH3Ź±ĖłµĆ°±Ė®µÄÅØ¶Č²»ŹĒ1 mol/L£¬Ö»ÓŠµ±22.4L NH3ČÜÓŚĖ®ÖʵĆ1L°±Ė®Ź±£¬ĘäÅØ¶Č²ÅŹĒ1 mol/L | |
| C£® | 10”ꏱ0.5 mol/LµÄĻ”ŃĪĖį100mL£¬Õō·¢µō5gĖ®£¬ĄäČ“µ½10”ꏱ£¬ĘäĢå»żŠ”ÓŚ100mL£¬ĖüµÄĪļÖŹµÄĮæÅØ¶Č“óÓŚ0.5 mol/L | |
| D£® | 10”ꏱ0.5 mol/LµÄKCl±„ŗĶČÜŅŗ100mL£¬Õō·¢µō5gĖ®£¬ĄäČ“µ½10”ꏱ£¬ĘäĢå»żŠ”ÓŚ100 mL£¬ĖüµÄĪļÖŹµÄĮæÅضČČŌĪŖ0.5 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĖį | B£® | ¼×±½ | C£® | ¼×“¼ | D£® | ĖÄ·śŅŅĻ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉżøßĪĀ¶Č”¢½µµĶŃ¹Ē攢Ōö¼ÓµŖĘų | B£® | ½µµĶĪĀ¶Č”¢Ōö“óŃ¹Ē攢¼ÓČė“߻ƼĮ | ||
| C£® | ÉżøßĪĀ¶Č”¢Ōö“óŃ¹Ē攢Ōö¼ÓµŖĘų | D£® | ½µµĶĪĀ¶Č”¢Ōö“óŃ¹Ē攢·ÖĄė³ö²æ·Ö°± |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaClµÄµē×ÓŹ½£ŗ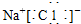 | B£® | ŅŅĻ©½į¹¹¼ņŹ½£ŗCH2ØTCH2 | ||
| C£® | MgŌ×Ó½į¹¹Ź¾ŅāĶ¼£ŗ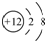 | D£® | ¼×ĶéµÄ½į¹¹Ź½£ŗ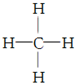 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«pH=4µÄ“×ĖįČÜŅŗĻ”ŹĶŗó£¬H+ÅضČŌö“ó | |
| B£® | ³£ĪĀĻĀ£¬0.01L pH=10µÄNaOHČÜŅŗ¼ÓĖ®Ļ”ŹĶµ½10L£¬“ĖŹ±ČÜŅŗµÄpH=7 | |
| C£® | øıäĢõ¼žŹ¹“×ĖįµÄµēĄėĘ½ŗāĻņÓŅŅĘ¶Æ£¬“×ĖįµÄµēĄė¶ČŅ»¶ØŌö“ó | |
| D£® | ³£ĪĀĻĀ0.1mol•L-1“×ĖįČÜŅŗµÄpH=a£¬¼ÓČėŹŹĮæµÄ“×ĖįÄĘ¹ĢĢåÄÜŹ¹ČÜŅŗpH=£Øa+1£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢Al3+”¢NO3-”¢SO42- | B£® | K+”¢Na+”¢CO32-”¢NO3- | ||
| C£® | MnO4-”¢K+”¢SO42-”¢Na+ | D£® | K+”¢Mg2+”¢SO32-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
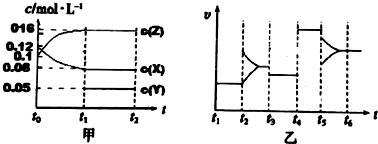
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com