
| A. | 物质跟氧气反应 | |
| B. | 有氧原子得失的反应 | |
| C. | 有元素化合价升降的反应 | |
| D. | 有电子得失或共用电子对发生偏移的反应 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 50% | B. | 40% | C. | 60% | D. | 30% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中$\frac{c(C{H}_{3}COO)}{c(C{H}_{3}COOH)•c(OH)}$不变 | |
| C. | 醋酸的电离程度增大,c(H+ )也增大 | |
| D. | 再加入 10mL0.1mol/L 的 NaOH 溶液,混合液的 pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl═H++Cl- | B. | H2SO4═2H++SO42- | C. | FeCl3═Fe3++Cl- | D. | NaOH═Na++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 偏铝酸钠溶液中加入一定量的盐酸,最终一定得到Al(OH)3沉淀 | |
| B. | 钠在敞口容器中存放或在空气中燃烧的产物都是Na2O2 | |
| C. | 向NaOH溶液中通入少量CO2或过量CO2都只生成Na2CO3 | |
| D. | 氯化铝和少量的氨水或过量的氨水反应都得到Al(OH)3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体有丁达尔效应 | |
| B. | B、胶体粒子直径在1nm-100nm之间 | |
| C. | 胶体粒子很小,不受重力作用 | |
| D. | 同种胶体粒子带同种电荷,它们之间互相排斥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应的反应热与反应的途径有关 | |
| B. | 电解过程中,化学能转化为电能而“储存”起来 | |
| C. | 强电解质溶液的导电能力一定强于弱电解质溶液 | |
| D. | 化学平衡常数的表达式与化学反应方程式的书写有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
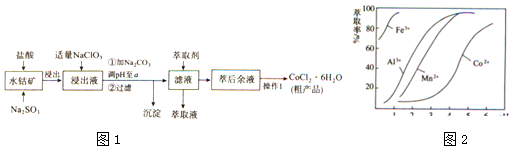
| 淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com