
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的沸点为H2T<H2R | B. | 单质与稀盐酸反应的快慢为L<Q | ||
| C. | M与T形成的化合物是离子化合物 | D. | L2+与R2-的核外电子数相等 |
分析 短周期元素中,R、T都有-2价,原子半径R>T,故R为S元素、T为O元素,L、Q元素有+2,处于ⅡA族,L原子半径较大,故L为Mg、Q为Be;M化合价为+3价,处于ⅢA族,原子半径介于Mg与S之间,M为Al.
A.水分子之间存在氢键,沸点较高;
B.金属性越强,金属与酸反应越剧烈;
C.氧化铝属于离子化合物;
D.核外电子数=质子数-离子带的电荷.
解答 短周期元素中,R、T都有-2价,原子半径R>T,故R为S元素、T为O元素,L、Q元素有+2,处于ⅡA族,L原子半径较大,故L为Mg、Q为Be;M化合价为+3价,处于ⅢA族,原子半径介于Mg与S之间,M为Al.
A.水分子之间存在氢键,沸点较高,故A错误;
B.金属性Mg比Be强,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为L>Q,故B错误;
C.M与T形成的化合物是氧化铝,属于离子化合物,故C正确;
D.Mg2+的核外电子数为12-2=10,S2-的核外电子数为16-(-2)=18,核外电子数不相等,故D错误,
故选:C.
点评 本题考查结构性质位置关系应用,根据原子半径及化合价来推断元素是解题的关键,熟悉掌握同周期、同主族元素性质递变规律,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 葡萄糖和果糖的分子式均为C6H12O6,二者互为同系物 | |
| D. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
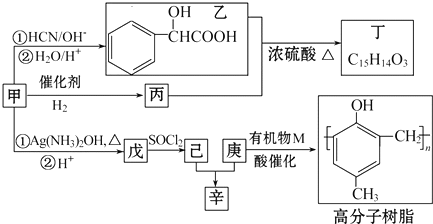

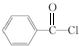 ,丁
,丁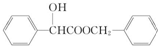 .
.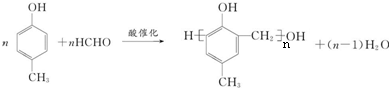 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 | |
| B. | 研发易降解的生物农药有利于环境保护 | |
| C. | 做衣服的棉、麻、蚕丝的成分都是纤维素 | |
| D. | 常用无水酒精来消毒,是因为酒精能够使细菌蛋白发生变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
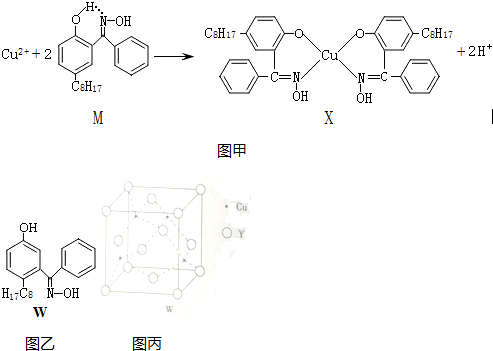
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | 镁浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 | 有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 | 剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 | 反应不十分剧烈;产生无色气体 |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 | 生成白色胶状沉淀,继而沉淀消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H与D | B. | CH3CH2OH与CH3COOH | ||
| C. | CH≡CH与C6H6 | D. | CH3CH2CH2CH3与 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 装置 | 现象 | 结论及解释 |
 | ①A试管中黑色沉淀逐渐溶解 ②A试管上方出现红棕色气体 ③B试管中出现白色沉淀 | a.现象②说明褐色沉淀具有 还原性. b.试管B中产生白色沉淀的总反应的离子方程式为 NO2+SO2+Ba2++H2O=BaSO4↓+NO+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 含有金属阳离子的晶体一定是离子晶体 | |
| B. | 化合物硫氰化铁和氢氧化二氨合银中都存在配位键 | |
| C. | KCl、HF、CH3CH2OH、SO2都易溶于水,且原因相同 | |
| D. | MgO的熔点比NaCl的高,主要是因为MgO的晶格能大于NaCl的晶格能. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com