
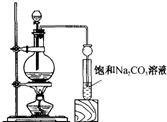
 实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇和少量浓硫酸混合,然后经分液漏斗边滴加醋酸边加热蒸馏,直接收集蒸馏产品可得到含有乙醇、乙醚、醋酸、少量水的乙酸乙酯粗产品.据此回答问题:
实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇和少量浓硫酸混合,然后经分液漏斗边滴加醋酸边加热蒸馏,直接收集蒸馏产品可得到含有乙醇、乙醚、醋酸、少量水的乙酸乙酯粗产品.据此回答问题:| 浓硫酸 |
| 170℃ |


科目:高中化学 来源: 题型:
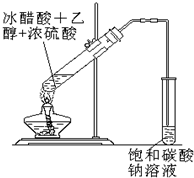 实验室合成乙酸乙酯粗产品的简易装置如右,由该实验可以得到乙酸乙酯粗产品.据此填空:
实验室合成乙酸乙酯粗产品的简易装置如右,由该实验可以得到乙酸乙酯粗产品.据此填空:| 催化剂 |
| 催化剂 |
| 催化剂 |
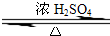 CH3COOCH2CH3+H2O,酯化反应
CH3COOCH2CH3+H2O,酯化反应| 催化剂 |
| 催化剂 |
| 催化剂 |
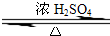 CH3COOCH2CH3+H2O,酯化反应
CH3COOCH2CH3+H2O,酯化反应查看答案和解析>>
科目:高中化学 来源: 题型:
实验室合成乙酸乙酯粗产品的步骤如下:

在蒸馏烧瓶内将过量的乙醇和少量浓H2SO4混合,然后经分液漏斗边滴加醋酸,边加热蒸馏,直接收集蒸馏产品可得到含有乙醇、乙醚、醋酸、少量水的乙酸乙酯粗产品。据此回答问题:
(1)反应中加入的乙醇是过量的,其目的是
________________________________。
(2)边滴加醋酸,边加热蒸馏的目的是
_________________________________。
(3)该实验中使用球形管除起冷凝作用外,另一重要作用是___________。
(4)试管中饱和碳酸钠溶液的作用是___________________; _______________;_____________________________。
(5)实验生成的乙酸乙酯,其密度比水_______(填“大”、“小”),有_________ 气味。
(6)实验中若温度过高(达170℃),副产物中主要有机产物是__________(填名称)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省嘉兴一中高二10月月考化学试卷(带解析) 题型:实验题
已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5 77.1℃ C2H5OC2H5(乙醚) 34.5℃ C2H5OH 78.3℃ CH3COOH 118℃ 实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸、边加热蒸馏。得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)反应中加入乙醇是过量的,其目的是: 。
将粗产品再经下列步骤精制:
(2)为除去其中的醋酸,可向产品中加入__________(填字母)。
A 无水乙醇 B 碳酸钠粉末 C 无水醋酸钠
(3)再向其中加入饱和氯化钙溶液,振荡。其目的是: 。
(4)然后再向其中加入无水硫酸钠,振荡。其目的是: 。
最后,将经过上述处理后的液体放入另一干燥的蒸馏瓶内,再蒸馏。弃去低沸点馏分,收集76~78℃沸程之间的馏分即得。
查看答案和解析>>
科目:高中化学 来源:2012届重庆市高二下学期期中考试化学试卷 题型:实验题
(11分) 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5 77.1℃ C2H5OC2H5(乙醚) 34.5℃ C2H5OH 78.3℃ CH3COOH 118℃ 实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸、边加热蒸馏。得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)写出合成乙酸乙酯的反应原理:____________________________________________。
(2)反应中加入乙醇是过量的,其目的是: 。
将粗产品再经下列步骤精制:
(3)为除去粗产品其中的醋酸,可向产品中加入__________(填字母)。
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(4)再向其中加入饱和氯化钙溶液,振荡。其目的是: 。
(5)最后,将经过上述处理后的液体放入另一干燥的蒸馏瓶内,再蒸馏。蒸馏时,需要的玻璃仪器有:酒精灯、温度计、冷凝管、锥形瓶、尾接管和____________。冷凝管的水流方向为 进 出,弃去低沸点馏分,收集76—78℃沸程之间的馏分即得。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com