
| A. | Cu、Fe、Ag | B. | Cl、Br、I | C. | Na、Cu、Hg | D. | F、Br、I |
分析 A.Cu不能置换出Fe;
B.氯气与NaBr发生置换反应生成溴,溴与NaI发生置换反应生成碘;
C.Na不能置换出Cu;
D.F不能置换出Br.
解答 解:A.Cu不能置换出Fe,因Fe比Cu活泼,故A不选;
B.氯气与NaBr发生置换反应生成溴,溴与NaI发生置换反应生成碘,则前面的元素可以把后面的元素从其化合物的溶液中置换出来,故B选;
C.Na不能置换出Cu,因Na与水反应生成NaOH和氢气,故C不选;
D.F不能置换出Br,因F的单质与水反应生成HF和氧气,故D不选;
故选B.
点评 本题考查金属的性质,为高频考点,把握金属活泼性及发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用右图所示装置进行有关实验.请回答下列问题:
某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用右图所示装置进行有关实验.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
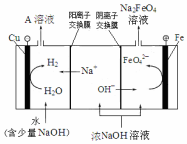 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3既是氧化剂又是还原剂 | B. | 氢元素既被氧化又被还原 | ||
| C. | 0.5mol氢气生成时转移1mol电子 | D. | 镁具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焰色反应是黄色 | |
| B. | 溶液有咸味 | |
| C. | 取少量溶液于试管中,滴加稀硝酸酸化的硝酸银溶液,出现白色沉淀 | |
| D. | 既出现A中的现象,又出现C中的现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com