
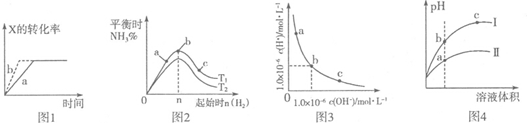
| A. | 图l所示,反应:X(g)+2Y(g)═3Z(g),b的压强一定比a大 | |
| B. | 图2表示合成氨反应,温度T1和T2对应的平衡常数为K1、K2,则:T1<T2,K1>K2 | |
| C. | 图3表明,该温度下,加入FeCl3不可能引起由b向a的变化 | |
| D. | 图4所示,用水稀释pH相同的盐酸和醋酸,I表示盐酸,Ⅱ表示醋酸,且溶液导电性:c>b>a |
分析 A、b曲线表示的反应比a反应速率快,平衡不移动;
B、合成氨的反应为放热反应,温度越高,平衡左移,氨气的百分含量越小;
C、温度不变,Kw不变,而氯化铁溶于水后水解显酸性;
D、图象分析,醋酸是弱电解质存在电离平衡,稀释相同倍数,强酸pH变化大.
解答 解:A、图1所示反应:X(g)+2Y(g)?3Z(g),b曲线表示的可以是增大压强,还可能是使用催化剂,故A错误;
B、合成氨的反应为放热反应,温度越高,平衡左移,氨气的百分含量越小,根据图象可知,温度T1<T2,而氨气的百分含量越高,说明平衡向右进行的程度越大,则K值越大,故有:K1>K2,故B正确;
C、温度不变,Kw不变,而氯化铁溶于水后水解显酸性,故氯化铁溶于水后溶液中的c(H+)变大,而c(OH-)变小,即可以由a转化为b点,故C错误;
D、图象分析,醋酸是弱电解质存在电离平衡,稀释相同倍数,强酸pH变化大,Ⅰ表示盐酸,Ⅱ表示醋酸,导电性a>b>c,故D错误.
故选B.
点评 本题考查了图象分析判断的能力,主要是化学反应有些因素的分析理解,饱和溶液的质量分数分析判断,弱电解质电离平衡的分析应用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 水蒸气通过Na2O2固体 | B. | 镁粉投入FeCl3溶液中 | ||
| C. | 铝粉与Fe2O3发生铝热反应 | D. | 焦炭在电炉中还原二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ②④⑤ | C. | ①②③⑤ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2与于恒容容器中生成1molN2O4 | B. | NO2与于恒压容器中生成1molN2O4 | ||
| C. | N2O4与于恒容容器中生成1molNO2 | D. | N2O4与于恒压容器中生成1molNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定是甲烷与乙烷的混合物 | B. | 可能是甲烷与丙烷的混合物 | ||
| C. | 一定含有乙烷 | D. | 可能是甲烷与己烷的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 相对密度(20℃) | 熔点 | 沸点 | 溶解性 | |
| A | 0.7893 | -117.3°C | 78.5°C | 与水以任意比混溶 |
| B | 0.7137 | -116.6°C | 34.5°C | 不溶于水 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com