
【题目】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示。

(1)若A为强碱,C、D常被用做食用“碱”。C → D反应的离子方程式为 ______________。
(2)若A为使用最广泛的金属单质,B是某强酸的稀溶液,则检验D溶液中金属阳离子的试剂为_____________,D → C反应的离子方程式为___________。
(3)若A为非金属单质,D是空气中的主要温室气体。D还可以转化为A,写出该反应的化学方程式_________。
【答案】CO32- + CO2 + H2O = 2HCO3- KSCN溶液 2Fe3+ + Fe = 3Fe2+ 2Mg + CO2![]() 2MgO + C
2MgO + C
【解析】
(1)若A为强碱,C、D常被用做食用“碱”,应为碳酸钠和碳酸氢钠,根据反应流程可知,A为氢氧化钠,与少量二氧化碳反应生成C为碳酸钠,与足量二氧化碳反应生成D为碳酸氢钠,碳酸钠溶液通入二氧化碳反应生成碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠和水;
(2)若A为使用最广泛的金属单质,B是某强酸的稀溶液,根据流程可推知A为铁,B为硝酸,过量的铁与稀硝酸反应生成C为硝酸亚铁,少量的铁与稀硝酸反应生成D为硝酸铁,硝酸亚铁与硝酸反应生成硝酸铁,硝酸铁与铁反应生成硝酸亚铁;
(3)若A为非金属单质,D是空气中的主要温室气体CO2。根据流程可知A为碳,碳在氧气不足的条件下燃烧生成C为CO,在氧气充足时燃烧生成D为CO2,CO在氧气中燃烧生成CO2,CO2与C在高温条件下反应生成CO。
(1)若A为强碱,C、D常被用做食用“碱”,应为碳酸钠和碳酸氢钠,根据反应流程可知,A为氢氧化钠,与少量二氧化碳反应生成C为碳酸钠,与足量二氧化碳反应生成D为碳酸氢钠,碳酸钠溶液通入二氧化碳反应生成碳酸氢钠,碳酸氢钠与氢氧化钠反应生成碳酸钠和水,故C → D反应的离子方程式为CO32- + CO2 + H2O = 2HCO3-;
(2)若A为使用最广泛的金属单质,B是某强酸的稀溶液,根据流程可推知A为铁,B为硝酸,过量的铁与稀硝酸反应生成C为硝酸亚铁,少量的铁与稀硝酸反应生成D为硝酸铁,硝酸亚铁与硝酸反应生成硝酸铁,硝酸铁与铁反应生成硝酸亚铁,则检验D溶液中金属阳离子Fe3+的试剂为KSCN溶液,D → C反应的离子方程式为2Fe3+ + Fe = 3Fe2+;
(3)若A为非金属单质,D是空气中的主要温室气体CO2。根据流程可知A为碳,碳在氧气不足的条件下燃烧生成C为CO,在氧气充足时燃烧生成D为CO2,CO在氧气中燃烧生成CO2,CO2与C在高温条件下反应生成CO,D还可以转化为A,是镁在二氧化碳中燃烧生成氧化镁和C,反应的化学方程式为2Mg + CO2![]() 2MgO + C。
2MgO + C。


科目:高中化学 来源: 题型:
【题目】香草醛又名香兰素,是食品和药品的重要原料,其结构简式如图所示。下列有关香草醛的说法中不正确的是( )
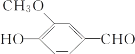
A.香草醛可以发生银镜反应
B.在一定条件下1mol香草醛可以与4molH2反应
C.香草醛遇FeCl3溶液可变色
D.香草醛可与NaOH溶液反应,也可与NaHCO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe、Cu、Cr都是第四周期过渡元素,回答下列问题。
(1)FeCl3是一种常用的净水剂,Cl元素的原子核外有___种不同运动状态的电子;有___种不同能级的电子,基态Fe3+的电子排布式为___。
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+。FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是___;K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的![]() 结构如图所示(K+未画出),则一个晶胞中的K+个数为___。
结构如图所示(K+未画出),则一个晶胞中的K+个数为___。

(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:![]() ,该配离子中含有的化学键类型有___(填字母)。
,该配离子中含有的化学键类型有___(填字母)。
a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有___个σ键,C原子的杂化方式为___。
(4)金属铜的晶胞为面心立方最密堆积,边长为361pm。则铜原子的直径约为___pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置进行乙醇氧化反应的探究实验,以下叙述错误的是( )
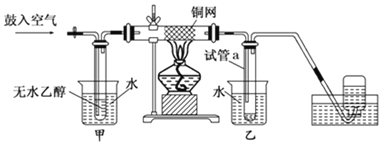
A.铜网表面乙醇发生氧化反应
B.甲、乙烧杯中的水均起冷却作用
C.试管a收集到的液体中至少有两种有机物
D.实验开始后熄灭酒精灯,铜网仍能红热,说明发生的是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
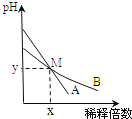
A.稀释前,![]()
B.稀释前,A溶液中由水电离出的![]() 的浓度大于
的浓度大于![]()
C.用醋酸中和A溶液至恰好完全反应时,溶液的pH为7
D.在M点,A、B两种碱溶液中阳离子的物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 A 含有碳、氢、氧三种元素,其质量比是 3:1:4,B 是最简单的芳香烃,D 是有芳香气味的酯。它们之间的转换关系如下:

回答下列问题:
(1)A 的结构简式为__________________________________________。
(2)C 中的官能团为__________________________________________。
(3) ![]() 的一氯代物有_________________________________________种。(不考虑立体异构)
的一氯代物有_________________________________________种。(不考虑立体异构)
(4)反应④的化学方程式为______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列叙述错误的是
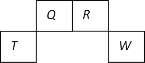
A.元素的非金属性:Q 强于 W
B.T 的氧化物能与 NaOH 溶液反应
C.R 元素的气态氢化物能与其最高价氧化物对应的水化物反应
D.Q 和 W 元素形成化合物 QW2分子中,各原子的最外层均满足 8 电子的稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下密闭容器中的反应:2A(g)+B(g)![]() 2C(g) △H<0达到平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是( )
2C(g) △H<0达到平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是( )

x | y | |
A | 再加入A | B的转化率 |
B | 再加入C | A的体积分数 |
C | 增大体积 | A的转化率 |
D | 升高温度 | 混合气体的平均摩尔质量 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多硫化钠Na2Sx(x≥2)在NaOH溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的物质的量之比为1:16.Na2Sx在结构上与Na2O2相似.则下列有关说法正确的是( )
A.该反应中Na2Sx是氧化剂,NaClO是还原剂
B.Na2Sx含有离子键和极性共价键
C.1molNa2Sx参加反应,有32mol电子转移
D.Na2Sx中的x数值为2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com