
”¾ĢāÄæ”æ½¹ŃĒĮņĖįÄĘ£ØNa2S2O5£©ŌŚŅ½Ņ©”¢Ļš½ŗ”¢Ó”Č¾”¢Ź³Ę·µČ·½ĆęÓ¦ÓĆ¹ć·ŗ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Éś²śNa2S2O5£¬Ķس£ŹĒÓÉNaHSO3¹ż±„ŗĶČÜŅŗ¾½į¾§ĶŃĖ®ÖʵƔ£Š“³öøĆ¹ż³ĢµÄ»Æѧ·½³ĢŹ½__________”£
£Ø2£©ĄūÓĆŃĢµĄĘųÖŠµÄSO2Éś²śNa2S2O5µÄ¹¤ŅÕĪŖ£ŗ
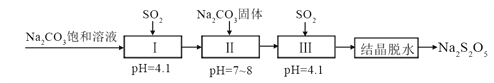
¢ŁpH=4.1Ź±£¬¢ńÖŠĪŖ__________ČÜŅŗ£ØŠ“»ÆѧŹ½£©”£
¢Ś¹¤ŅÕÖŠ¼ÓČėNa2CO3¹ĢĢ唢²¢ŌŁ“Ī³äČėSO2µÄÄæµÄŹĒ__________”£
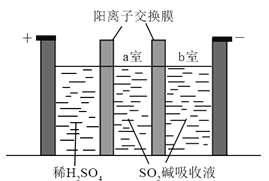
£Ø3£©ÖʱøNa2S2O5Ņ²æɲÉÓĆČżŹŅĤµē½ā¼¼Źõ£¬×°ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠSO2¼īĪüŹÕŅŗÖŠŗ¬ÓŠNaHSO3ŗĶNa2SO3”£Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖ_____________”£µē½āŗó£¬__________ŹŅµÄNaHSO3ÅضČŌö¼Ó”£½«øĆŹŅČÜŅŗ½ųŠŠ½į¾§ĶŃĖ®£¬æɵƵ½Na2S2O5”£
£Ø4£©Na2S2O5æÉÓĆ×÷Ź³Ę·µÄæ¹Ńõ»Æ¼Į”£ŌŚ²ā¶ØijĘĻĢŃ¾ĘÖŠNa2S2O5²ŠĮōĮæŹ±£¬Č”50.00 mLĘĻĢŃ¾Ęѳʷ£¬ÓĆ0.01000 mol”¤L1µÄµā±ź×¼ŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄ10.00 mL”£µĪ¶Ø·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____________£¬øĆѳʷ֊Na2S2O5µÄ²ŠĮōĮæĪŖ____________g”¤L1£ØŅŌSO2¼Ę£©”£
”¾“š°ø”æ 2NaHSO3£½Na2S2O5+H2O NaHSO3 µĆµ½NaHSO3¹ż±„ŗĶČÜŅŗ 2H2O£4e££½4H£«+O2”ü a S2O52£+2I2+3H2O£½2SO42£+4I£+6H£« 0.128
”¾½āĪö”æ·ÖĪö£ŗ£Ø1£©øł¾ŻŌ×ÓŹŲŗćŹéŠ“·½³ĢŹ½£»
£Ø2£©¢Łøł¾ŻČÜŅŗĻŌĖįŠŌÅŠ¶Ļ²śĪļ£»
¢ŚŅŖÖʱø½¹ŃĒĮņĖįÄĘ£¬ŠčŅŖÖʱøŃĒĮņĖįĒāÄĘ¹ż±„ŗĶČÜŅŗ£¬¾Ż“ĖÅŠ¶Ļ£»
£Ø3£©øł¾ŻŃō¼«ĒāŃõøł·Åµē£¬Ņõ¼«ĒāĄė×ӷŵē£¬½įŗĻŃōĄė×Ó½»»»Ä¤µÄ×÷ÓĆ½ā“š£»
£Ø4£©½¹ŃĒĮņĖįÄĘÓėµ„ÖŹµā·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬¾Ż“ĖŹéŠ“·½³ĢŹ½£»øł¾Ż·½³ĢŹ½¼ĘĖć²ŠĮōĮ攣
Ļź½ā£ŗ£Ø1£©ŃĒĮņĖįĒāÄĘ¹ż±„ŗĶČÜŅŗĶŃĖ®Éś³É½¹ŃĒĮņĖįÄĘ£¬øł¾ŻŌ×ÓŹŲŗćæÉÖŖ·“Ó¦µÄ·½³ĢŹ½ĪŖ2NaHSO3£½Na2S2O5+H2O£»
£Ø2£©¢ŁĢ¼ĖįÄʱ„ŗĶČÜŅŗĪüŹÕSO2ŗóµÄČÜŅŗĻŌĖįŠŌ£¬ĖµĆ÷Éś³ÉĪļŹĒĖįŹ½ŃĪ£¬¼“¢ńÖŠĪŖNaHSO3£»
¢ŚŅŖÖʱø½¹ŃĒĮņĖįÄĘ£¬ŠčŅŖÖʱøŃĒĮņĖįĒāÄĘ¹ż±„ŗĶČÜŅŗ£¬Ņņ“Ė¹¤ŅÕÖŠ¼ÓČėĢ¼ĖįÄĘ¹ĢĢ唢²¢ŌŁ“Ī³äČė¶žŃõ»ÆĮņµÄÄæµÄŹĒµĆµ½NaHSO3¹ż±„ŗĶČÜŅŗ£»
£Ø3£©Ńō¼«·¢ÉśŹ§Č„µē×ÓµÄŃõ»Æ·“Ó¦£¬Ńō¼«ĒųŹĒĻ”ĮņĖį£¬ĒāŃõøł·Åµē£¬Ōņµē¼«·“Ó¦Ź½ĪŖ2H2O£4e££½4H£«+O2”ü”£Ńō¼«ĒųĒāĄė×ÓŌö“ó£¬ĶعżŃōĄė×Ó½»»»Ä¤½ųČėaŹŅÓėŃĒĮņĖįÄĘ½įŗĻÉś³ÉŃĒĮņĖįÄĘ”£Ņõ¼«ŹĒĒāĄė×ӷŵē£¬ĒāŃõøłÅضČŌö“ó£¬ÓėŃĒĮņĖįĒāÄĘ·“Ӧɜ³ÉŃĒĮņĖįÄĘ£¬ĖłŅŌµē½āŗóaŹŅÖŠŃĒĮņĖįĒāÄʵÄÅضČŌö“ó”£
£Ø4£©µ„ÖŹµā¾ßÓŠŃõ»ÆŠŌ£¬ÄÜ°Ń½¹ŃĒĮņĖįÄĘŃõ»ÆĪŖĮņĖįÄĘ£¬·“Ó¦µÄ·½³ĢŹ½ĪŖS2O52£+2I2+3H2O£½2SO42£+4I£+6H£«£»ĻūŗĵāµÄĪļÖŹµÄĮæŹĒ0.0001mol£¬ĖłŅŌ½¹ŃĒĮņĖįÄĘµÄ²ŠĮōĮæ£ØŅŌSO2¼Ę£©ŹĒ![]() ”£
ӣ


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖijĖįH2BŌŚĖ®ČÜŅŗÖŠ“ęŌŚĻĀĮŠ¹ŲĻµ£ŗ¢Ł![]() ¢Ś
¢Ś![]() £¬¹ŲÓŚøĆĖį¶ŌÓ¦µÄĖįŹ½ŃĪNaHBµÄČÜŅŗ£¬ĻĀĮŠĖµ·ØÖŠ£¬Ņ»¶ØÕżČ·µÄŹĒ
£¬¹ŲÓŚøĆĖį¶ŌÓ¦µÄĖįŹ½ŃĪNaHBµÄČÜŅŗ£¬ĻĀĮŠĖµ·ØÖŠ£¬Ņ»¶ØÕżČ·µÄŹĒ
A. NaHBŹōÓŚČõµē½āÖŹ
B. ČÜŅŗÖŠµÄĄė×ÓÅضČc(Na+)>c(HB-)>c(H+)>c(OH-)
C. c(Na+)=c(HB-)+c(B2-)+c(H2B)
D. c(Na+)+c(H+)=c(HB-)+c(B2-)+c(OH-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖŹŅĪĀŹ±,0.1 mol”¤L£1ijŅ»ŌŖĖįHAŌŚĖ®ÖŠÓŠ0.1%·¢ÉśµēĄė,ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A. øĆČÜŅŗµÄpH£½4
B. ÉżøßĪĀ¶Č,ČÜŅŗµÄpHŌö“ó
C. “ĖĖįČÜŅŗµÄKW=1.0”Į10£14 mol2”¤L2£
D. ČōHB£«NaA£½HA£«NaBÄܽųŠŠ,ŌņKa£ØHB£©£¾Ka£ØHA£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮ×ĖįŃĒĢśļ®£ØLiFePO4£©µē³ŲŹĒŠĀÄÜŌ“Ęū³µµÄ¶ÆĮ¦µē³ŲÖ®Ņ»”£²ÉÓĆŹŖ·ØŅ±½š¹¤ŅÕ»ŲŹÕ·Ļ¾ÉĮņĖįŃĒĢśļ®µē³ŲÕż¼«Ę¬ÖŠµÄ½šŹō£¬ĘäĮ÷³ĢČēĻĀ£ŗ

ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A. ŗĻĄķ“¦Ąķ·Ļ¾Éµē³ŲÓŠĄūÓŚ±£»¤»·¾³ŗĶ׏Ō“ŌŁĄūÓĆ
B. “Ó”°Õż¼«Ę¬”±ÖŠæÉ»ŲŹÕµÄ½šŹōŌŖĖŲÓŠAl”¢Fe”¢Li
C. ”°³Įµķ”±·“Ó¦µÄ½šŹōĄė×ÓĪŖFe3+
D. ÉĻŹöĮ÷³ĢÖŠæÉÓĆĮņĖįÄĘ“śĢęĢ¼ĖįÄĘ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĀČĖ®ÖŠ“ęŌŚ¶ąÖÖ·Ö×ÓŗĶĄė×Ó£¬ĖüĆĒŌŚ²»Ķ¬µÄ·“Ó¦ÖŠ±ķĻÖ³öø÷×ŌµÄŠŌÖŹ”£ĻĀĮŠŹµŃéĻÖĻóŗĶ½įĀŪŅ»ÖĀĒŅÕżČ·µÄŹĒ£Ø £©
A. ¼ÓČėÓŠÉ«²¼Ģõ£¬Ņ»»į¶łÓŠÉ«²¼ĢõĶŹÉ«£¬ĖµĆ÷ČÜŅŗÖŠÓŠCl2“ęŌŚ
B. ČÜŅŗ³ŹĒ³»ĘĀĢÉ«£¬ĒŅÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬ĖµĆ÷ÓŠCl2·Ö×Ó“ęŌŚ
C. ÓĆŃĪĖįĖį»Æŗ󣬵ĪČėAgNO3ČÜŅŗ²śÉś°×É«³Įµķ£¬ĖµĆ÷ĀČĖ®ÖŠÓŠCl-“ęŌŚ
D. ¼ÓČėNaOHČÜŅŗ£¬ĀČĖ®»ĘĀĢÉ«ĻūŹ§£¬ĖµĆ÷ÓŠHClO·Ö×Ó“ęŌŚ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±ź×¼×“æöĻĀ,aLHClČÜÓŚ1000gĖ®ÖŠ,µĆµ½µÄŃĪĖįĆܶČĪŖbg”¤mL£1,ŌņøĆŃĪĖįÅØ¶ČŹĒ£ŗ
A£®a/22.4 mol”¤L£1
B£®ab/22400 mol”¤L£1
C£®ab/£Ø22400+36.5£© mol”¤L£1
D£®1000ab/£Ø22400+36.5a£© mol”¤L£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ"Ą¬»ųŹĒ·Å“ķĮĖĪ»ÖƵÄ׏Ō“",Ó¦øĆ·ÖĄą»ŲŹÕĄūÓĆ.Éś»īÖŠ·ĻĘśµÄĢś¹ų,ĀĮÖĘŅץ¹Ž,Ķµ¼ĻßµČæÉŅŌ¹éĪŖŅ»Ąą¼ÓŅŌ»ŲŹÕ,ĖüĆĒŹōÓŚ( )
A. ÓŠ»śĪļ B. Ńõ»ÆĪļ C. ŃĪ D. ½šŹō»ņŗĻ½š
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)ÓĆĖ«ĻßĒŷرķŹ¾ĻĀĮŠŃõ»Æ»¹Ō·“Ó¦£¬²¢Öø³öŃõ»Æ¼ĮŗĶ»¹Ō¼Į”£Zn£«H2SO4(Ļ”)===ZnSO4£«H2”ü_____________________________________£¬Ńõ»Æ¼Į__________£»»¹Ō¼Į______________”£
(2)ÓƵ„ĻßĒŷرķŹ¾ĻĀĮŠŃõ»Æ»¹Ō·“Ó¦£¬²¢Öø³öŃõ»Æ¼ĮŗĶ»¹Ō¼Į”£Fe2O3£«3CO![]() 2Fe£«3CO2______________________________________________£¬Ńõ»Æ¼Į__________£»»¹Ō¼Į__________”£
2Fe£«3CO2______________________________________________£¬Ńõ»Æ¼Į__________£»»¹Ō¼Į__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČżĀČĒā¹č£ØSiHCl3£©ŹĒÖʱø¹čĶ锢¶ą¾§¹čµÄÖŲŅŖŌĮĻ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©SiHCl3ŌŚ³£ĪĀ³£Ń¹ĻĀĪŖŅ×»Ó·¢µÄĪŽÉ«ĶøĆ÷ŅŗĢ壬Óö³±ĘųŹ±·¢ŃĢÉś³É(HSiO)2OµČ£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½__________”£
£Ø2£©SiHCl3ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦£ŗ
2SiHCl3(g)![]() SiH2Cl2(g)+ SiCl4(g) ¦¤H1=48 kJ”¤mol1
SiH2Cl2(g)+ SiCl4(g) ¦¤H1=48 kJ”¤mol1
3SiH2Cl2(g)![]() SiH4(g)+2SiHCl3 (g) ¦¤H2=30 kJ”¤mol1
SiH4(g)+2SiHCl3 (g) ¦¤H2=30 kJ”¤mol1
Ōņ·“Ó¦4SiHCl3(g)![]() SiH4(g)+ 3SiCl4(g)µÄ¦¤H=__________ kJ”¤mol1”£
SiH4(g)+ 3SiCl4(g)µÄ¦¤H=__________ kJ”¤mol1”£
£Ø3£©¶ŌÓŚ·“Ó¦2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)£¬²ÉÓĆ“óæ×Čõ¼īŠŌŅõĄė×Ó½»»»Ź÷Ö¬“߻ƼĮ£¬ŌŚ323 KŗĶ343 KŹ±SiHCl3µÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄ½į¹ūČēĶ¼ĖłŹ¾”£
SiH2Cl2(g)+SiCl4(g)£¬²ÉÓĆ“óæ×Čõ¼īŠŌŅõĄė×Ó½»»»Ź÷Ö¬“߻ƼĮ£¬ŌŚ323 KŗĶ343 KŹ±SiHCl3µÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄ½į¹ūČēĶ¼ĖłŹ¾”£
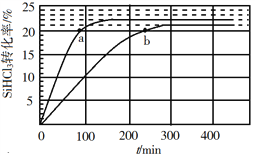
¢Ł343 KŹ±·“Ó¦µÄĘ½ŗā×Ŗ»ÆĀŹ¦Į=_________%”£Ę½ŗā³£ŹżK343 K=__________£Ø±£Įō2Ī»Š”Źż£©”£
¢ŚŌŚ343 KĻĀ£ŗŅŖĢįøßSiHCl3×Ŗ»ÆĀŹ£¬æɲÉČ”µÄ“ėŹ©ŹĒ___________£»ŅŖĖõ¶Ģ·“Ó¦“ļµ½Ę½ŗāµÄŹ±¼ä£¬æɲÉČ”µÄ“ėŹ©ÓŠ____________”¢___________”£
¢Ū±Č½Ļa”¢b“¦·“Ó¦ĖŁĀŹ“󊔣ŗ¦Ōa________¦Ōb£ØĢī”°“óÓŚ”±”°Š”ÓŚ”±»ņ”°µČÓŚ”±£©”£·“Ó¦ĖŁĀŹ¦Ō=¦ŌÕż¦ŌÄę=![]()
![]() £¬kÕż”¢kÄę·Ö±šĪŖÕż”¢ÄęĻņ·“Ó¦ĖŁĀŹ³£Źż£¬xĪŖĪļÖŹµÄĮæ·ÖŹż£¬¼ĘĖća“¦
£¬kÕż”¢kÄę·Ö±šĪŖÕż”¢ÄęĻņ·“Ó¦ĖŁĀŹ³£Źż£¬xĪŖĪļÖŹµÄĮæ·ÖŹż£¬¼ĘĖća“¦![]() =__________£Ø±£Įō1Ī»Š”Źż£©”£
=__________£Ø±£Įō1Ī»Š”Źż£©”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com