
| A. | C6H5CH2Cl+NaCN→C6H5CH2CN+NaCl | |
| B. | C6H5Li+CO2→C6H5COOLi | |
| C. | CH3CH2CHO+HCN$\stackrel{NaOH}{→}$ | |
| D. | CH3COOCH2CH3$→_{气相}^{450℃}$CH3COOH+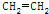 |
分析 有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,
取代反应指有机化合物分子中原子或原子团被其它原子或原子团所取代的反应;结合选项中发生的反应判断.
解答 解:A、C6H5CH2Cl+NaCN→C6H5CH2CN+NaCl是C6H5CH2Cl中氯原子被CN基所取代,属于取代反应,故A不选;
B、C6H5Li+CO2→C6H5COOLi,只有一种生成物,应为加成反应,故B不选;
C、CH3CH2CHO+HCN→$\stackrel{NaOH}{→}$CH3CH2CH(CN)OH是CH3CH2CHO中碳氧双键发生断裂,两个碳原子分别结合了氢原子和CN基,属于加成反应,故C不选;
D、CH3COOCH2CH3$→_{气相}^{450℃}$CH3COOH+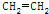 ,既不属于加成反应,也不属于取代反应,故D选;
,既不属于加成反应,也不属于取代反应,故D选;
故选:D.
点评 本题主要考查了加成反应与取代反应的判断,加成反应的条件是有机物中必须含有不饱和键(如碳碳双键、碳氧双键、碳碳三键等).


 互动课堂系列答案
互动课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | X的原子半径大于Y | |
| B. | 若X为ⅠA族元素,则该化合物中含离子键 | |
| C. | 若X2Y的焰色为黄色,则它的电子式是 | |
| D. | 若每个X2Y分子中含有10个电子,则Y是第3周期元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加C的用量 | B. | 增大反应体系的压强使体积改变 | ||
| C. | 升高体系的反应温度 | D. | 将容器的体积缩小一半 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气与水反应:Cl2+H2O=2H++Cl-+ClO- | |
| B. | 碳酸氢钙溶液加到盐酸中:Ca(HCO3)2+2HCl=Ca2++2CO2↑+2H2O | |
| C. | 少量金属钠加到冷水中:Na+2H2O=Na++OH-+H2↑ | |
| D. | 氢氧化铜加到盐酸中:Cu(OH)2+2H+=Cu2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物.PM2.5被吸入人体后会直接进入支气管,易引发包括哮喘、支气管炎和心血管病等方面的疾病 | |
| B. | 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| C. | 利用二氧化碳等原料合成的聚碳酸酯类可降解塑料替代聚乙烯塑料 | |
| D. | 生物柴油的主要成分是利用从泔水中提取的地沟油与甲醇反应生成的脂肪酸甲酯类化合物,与石化柴油有本质不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑧⑨ | B. | ②④⑤⑦⑨ | C. | ①③⑥⑧⑨ | D. | ③⑤⑥⑦⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com