
分析 (1)复分解反应是两种化合物中的阴阳离子之间交换成分的反应;酸碱中和反应属于放热反应;
(2)铵盐和氢氧化钡晶体之间的反应是吸热反应;
(3)自发地氧化还原反应可以设计成原电池;
(4)物质的燃烧反应可以设计成原电池;
(5)金属铜和硝酸银之间发生置换反应得到金属铜和硝酸银.
解答 解:(1)氢氧化钠与硫酸之间的反应属于复分解反应,也是中和反应,也是放热的,故答案为:①;
(2)八水合氢氧化钡与氯化铵之间的反应是吸热反应,故答案为:③;
(3)②一氧化碳与氧气的燃烧反应可以设计成燃料电池,金属铜与硝酸银间发生置换反应得到金属铜和硝酸银,属自发的氧化还原反应,可以设计成原电池,故答案为:②④;(4)一氧化碳与氧气的燃烧反应可以设计成燃料电池,故答案为:②;
(5)金属铜和硝酸银之间发生置换反应得到金属铜和硝酸银,即Cu+2Ag+═Cu2++2Ag,故答案为:Cu+2Ag+═Cu2++2Ag.
点评 本题考查学生复分解反应、置换反应类型的特点、原电池的构成条件以及反应式的书写等方面的知识,属于综合知识的考查,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
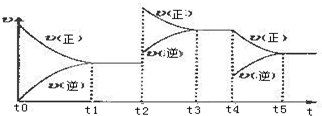
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
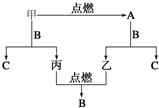 甲、乙、丙三种常见单质,A、B、C是三种常见的化合物,A为淡黄色固体,它们之间的转化关系如图所示.
甲、乙、丙三种常见单质,A、B、C是三种常见的化合物,A为淡黄色固体,它们之间的转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 电 极 | Zn C | Cu Ag | Zn Cu | Fe Zn |
| 溶 液 | 硫酸 | 硝酸银 | 蔗糖 | 硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
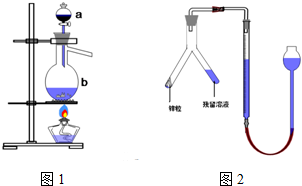
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
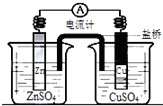
| A. | 铜是阳极,铜片上有气泡产生 | |
| B. | 锌离子在锌片表面被还原 | |
| C. | 正极附近的SO${\;}_{4}^{2-}$离子浓度逐渐增大 | |
| D. | 盐桥中的阳离子会移向CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
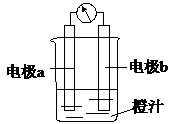 课堂学习中,同学们利用镁条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成.下列结论不正确的是( )
课堂学习中,同学们利用镁条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成.下列结论不正确的是( )| A. | 原电池是将化学能转化成电能的装置 | |
| B. | 原电池由电极、电解质溶液和导线等组成 | |
| C. | 右图中a极为镁条、b极为锌片时,导线中会产生电流 | |
| D. | 右图中a极为锌片、b极为铜片时,电子由铜片通过导线流向锌片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅是制造光电池的主要原料 | |
| B. | 硅是现代光学及光纤制品的基本原料 | |
| C. | 可用石英坩埚加热氢氧化钠固体 | |
| D. | 在电子工业中,硅是重要的半导体材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com