
 欲配制250mL0.1mol/L的NaOH溶液,回答下列有关问题.
欲配制250mL0.1mol/L的NaOH溶液,回答下列有关问题.分析 (1)熟悉仪器构造说出其名称;依据容量瓶构造及使用注意事项解答;
(2)依据托盘天平使用方法结合氢氧化钠具有腐蚀性的特点解答,依据m=CVM计算溶质的质量;
(3)依据移液和定容的正确操作解答;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
解答 解:(1)如图仪器A的名称250mL容量瓶;容量瓶带有瓶塞,使用前应检查是否漏水;
故答案为:250mL容量瓶;漏水;
(2)托盘天平使用遵循:左物右码的原则,药品应放在左盘;氢氧化钠为腐蚀性药品,应放在小烧杯中称量;配制250mL0.1mol/L的NaOH溶液,应称取溶质氢氧化钠的质量m=0.25L×0.1mol/L×40g/mol=1.0g;
故答案为:左;小烧杯;1.0;
(3)转移溶液时,应将已冷却的NaOH溶液沿玻璃棒注入容量瓶,当A中的液面接近刻度1-2cm处,改用胶头滴管加水至标线;
故答案为:玻璃棒;胶头滴管;
(4)(a)若称量前NaOH已部分潮解,导致称取的固体中含有氢氧化钠的物质的量偏小,溶液浓度偏低;
(b)不将洗涤液转移入仪器A就定容,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低;
(c)定容时,仰视仪器A刻度线,导致溶液体积偏大,溶液浓偏低;
故答案为:偏低;偏低;偏低.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和配制步骤是解题关键,注意容量瓶规格的选择和误差分析方法,题目难度不大.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:多选题
| A. | 一定存在SO42-、CO32-、NH4+,可能存在K+、Cl-、Na+ | |
| B. | 一定存在SO42-、CO32-、NH4+、Na+、Cl-,一定不存在K+、Na+ | |
| C. | c(CO32-)=0.01 mol•L-1,c(NH4+)>c(SO42-) | |
| D. | 如果上述6种离子都存在,则c(Cl-)>c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
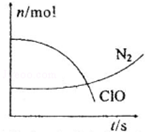
| A. | 还原剂是含CN-的物质,氧化产物不只有N2 | |
| B. | 氧化剂是ClO-,还原产物是HCO3- | |
| C. | 参与反应的氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 标准状况下若生成2.24LN2则转移电子1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 2mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 | |
| B. | 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 | |
| C. | 二氧化硫的催化氧化是放热反应,所以升高温度,反应速率减慢 | |
| D. | 汽车尾气中的CO和NO可以反应生成N2和CO2,在排气管中加催化剂可减小空气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图,烧杯中盛有等体积的水和煤油,现将一小块金属钠加入烧杯中,试推断能观察到的实验现象应是( )
如图,烧杯中盛有等体积的水和煤油,现将一小块金属钠加入烧杯中,试推断能观察到的实验现象应是( )| A. | 钠悬浮在煤油层中 | |
| B. | 钠静止在两液面之间 | |
| C. | 钠沉入水底下 | |
| D. | 钠熔化成闪亮的小球,在两液体界面附近上下跳动 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2CO3和NaHCO3形成的混合溶液中:2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| B. | 0.1mol•L-1NaHSO3溶液中通入NH3至溶液pH=7:c(Na+)>c(NH4+)>c(SO32-) | |
| C. | 物质的量浓度相等的:①(NH4)2SO4溶液、②NH4HCO3溶液、③NH4Cl溶液、④(NH4)2Fe(SO4)2溶液中c(NH4+)的大小关系:④>①>②>③ | |
| D. | 0.1mol•L-1CH3COONa溶液中通入HCl至溶液pH=7:c(Na+)>c(CH3COOH)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com