
| A. |  的名称是2,3-二甲基己烷 的名称是2,3-二甲基己烷 | |
| B. | 有机物CH3CO18OH和C2H5OH在浓硫酸催化作用下产物为CH3CO18OC2H5和H2O | |
| C. | 有机物 的一种芳香族同分异构体能发生银镜反应 的一种芳香族同分异构体能发生银镜反应 | |
| D. | 反应 属于加成反应,理论上该反应的原子利用率为100% 属于加成反应,理论上该反应的原子利用率为100% |
分析 A、烷烃命名时,要选最长的碳链为主链,然后从离支链近的一端给主链上的碳原子进行编号;
B、根据酯化反应的反应机理是“酸脱羟基醇脱氢”来分析;
C、要发生银镜反应,则结构中必须有醛基,根据不饱和度来分析;
D、根据加成反应原理对该有机物的反应类型进行判断,反应物原子完全转化成生成物;
解答 解:A、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,为己烷,然后从离支链近的一端给主链上的碳原子进行编号,则在3号和4号碳上各有一个甲级,故名称为:3,4-二甲基己烷,故A错误;
B、酯化反应的反应机理是“酸脱羟基醇脱氢”,故有机物CH3CO18OH和C2H5OH在浓硫酸催化作用下发生酯化反应时,18O应到水中,故产物为CH3COOC2H5和H218O,故B错误;
C、该有机物的不饱和度为$\frac{2×7+2-8}{2}$=4,则对应的一种芳香族同分异构体中只含有苯环,不含醛基,则不能发生银镜反应,故C错误.
D、反应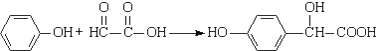 中,
中,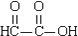 的醛基中碳氧双键断裂,不饱和键的碳氧双键变成饱和的单键,该反应属于加成反应,故D正确;
的醛基中碳氧双键断裂,不饱和键的碳氧双键变成饱和的单键,该反应属于加成反应,故D正确;
故选D.
点评 本题考查了有机物的命名、有机物结构与性质、有机反应类型的判断,题目难度中等,注意掌握常见有机物的结构与性质,明确常见有机物的命名原则及有机反应原理、反应类型.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
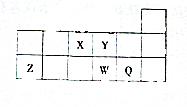 短周期元素X、Y、Z、W、Q在元素周期表中相对位置如图所示
短周期元素X、Y、Z、W、Q在元素周期表中相对位置如图所示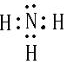 ,其水溶液呈碱性性(填酸、碱或中)
,其水溶液呈碱性性(填酸、碱或中)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 三氯氧磷(POCl3)常温下为无色液体,有广泛应用.近年来三氯氧磷的工业生产由三氯化磷的“氧气直接氧化法”代替传统的三氯化磷“氯化水解法”(由氯气、三氯化磷和水为原料反应得到).
三氯氧磷(POCl3)常温下为无色液体,有广泛应用.近年来三氯氧磷的工业生产由三氯化磷的“氧气直接氧化法”代替传统的三氯化磷“氯化水解法”(由氯气、三氯化磷和水为原料反应得到).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
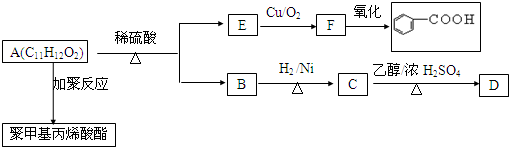
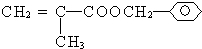 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾可用于海水的净化,但不能用于海水的淡化 | |
| B. | 使用清洁能源是防止酸雨的重要的措施 | |
| C. | 胃酸过多的病人均可服用含Al(OH)3或NaHCO3的药物进行治疗 | |
| D. | 84消毒液可用来漂白某些衣物,为加快漂白速度,使用时可加入少量稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 都能与NaOH溶液反应,每mol消耗NaOH的物质的量之比为1:1 | |
| B. | 都能与溴水反应,每mol消耗Br2的物质的量之比为3:2 | |
| C. | 都能与H2发生加成反应,每mol消耗H2的物质的量之比为4:7 | |
| D. | 都能与O2发生氧化反应,每mol消耗O2的物质的量之比为13:15 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D、E以原子个数比2:1形成的化合物,只含离子键 | |
| B. | 元素A、B、C的单质晶体可能属于同种类型的晶体,也可能是不同类型的晶体.如果B在A2B7CD分子中有四种不同的环境,则该分子不能与硫酸反应 | |
| C. | 含E的某种离子的水溶液,滴加某种含A、C或A、C、D元素组成的离子的溶液,均可生成配合物 | |
| D. | B与C形成的化合物其沸点一定高于A与B形成的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
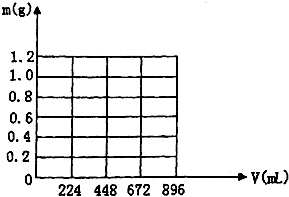 将KOH和Ca(OH)2混合物1.86g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO2的体积为224mL(标准状况,忽略CO2溶于水情况,以下情况相同.)
将KOH和Ca(OH)2混合物1.86g全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO2气体.当生成沉淀的质量刚好最大时,消耗CO2的体积为224mL(标准状况,忽略CO2溶于水情况,以下情况相同.)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可燃冰是可以燃烧的冰 | |
| B. | 明矾的化学式:KAl(SO4)2 | |
| C. | 酒精、水玻璃、福尔马林都是非电解质 | |
| D. | 肽键是蛋白质一级结构中的主键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com