
【题目】pH=0的某X溶液中,除H+外,还可能存在Al3+、Fe2+、NH4+、Ba2+、Cl-、CO32-、SO42-、NO3-中的若干种,现取适量X溶液进行如下一系列实验:
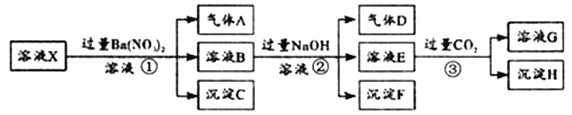
下列有关判断不正确的是( )
A. 生成气体A的离子方程式为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
B. 生成沉淀H的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
C. 溶液X中一定没有的离子仅为:CO32-、Ba2+
D. 溶液X中一定含有的离子是:H+、Fe2+、SO42-、NH4+、Al3+
【答案】C
【解析】强酸性溶液X,则溶液中不存在弱酸根离子CO32-,溶液和硝酸钡溶液反应生成沉淀C,则溶液中存在SO42-,不存在和硫酸根离子反应的Ba2+,C是BaSO4;酸性条件下硝酸根离子具有强氧化性,所以溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,则溶液中存在Fe2+,不存在NO3-,A是NO;溶液B中加入过量氢氧化钠溶液时,产生气体D,则溶液中含有NH4+,D是NH3,产生沉淀F是Fe(OH)3,溶液E通入过量二氧化碳时产生沉淀H和溶液G,则溶液中存在Al3+,沉淀H是Al(OH)3,溶液G是NaHCO3;A. 溶液X中应含有Fe2+,酸性条件下与硝酸根离子反应生成气体NO,反应的离子方程式为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,选项A正确;B. 生成沉淀H的离子方程式为:AlO2--+CO2+2H2O=Al(OH)3↓+HCO3-,选项B正确;C. 溶液X中一定没有的离子为:CO32-、Ba2+、NO3-,选项C错误;D. 溶液X中一定含有的离子是:H+、Fe2+、SO42-、NH4+、Al3+,选项D错误。答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列物质的变化,不能通过一步化学反应完成的是( )
A.Na2O2→Na2CO3B.Fe→FeCl2C.SiO2→H2SiO3D.Na2CO3→NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离NaCl和BaCl2两种固体混合物,回答下列问题:
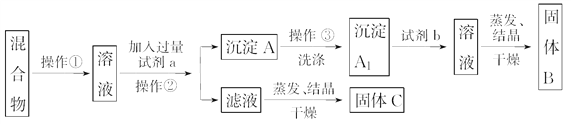
供选试剂:Na 2CO3溶液、Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作②的名称是______________。
(2)试剂a是________(填化学式,下同),试剂b是____________,固体B是________。
(3)加入试剂a所发生的化学反应方程式为_______________________________________。
(4)简述洗涤的操作步骤____________________________________________________________。
(5)该方案能否达到实验目的?___________。若不能,应如何改进(若能,此问不用回答)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式
(1)工业上制备氯乙烯_____________
(2)2-氯丙烷与KOH 的乙醇溶液共热____________
(3)实验室制乙烯__________
(4)中苯在铁粉催化下与溴单质反应__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过用水溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
A.硝酸钾、氢氧化钠B.氧化铜、二氧化锰
C.氯化钾、二氧化锰D.硫酸铜、氢氧化钡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同质量的![]() 气体和
气体和![]() 气体,其分子数之比为 ______ ,氧原子数之比为 ______ ,相同条件下
气体,其分子数之比为 ______ ,氧原子数之比为 ______ ,相同条件下![]() 同温同压
同温同压![]() 的体积之比为 ______ ,密度之比为 ______ .
的体积之比为 ______ ,密度之比为 ______ .
(2)![]() 与
与![]() 的混合气体中,氧元素的质量分数为
的混合气体中,氧元素的质量分数为![]() ,则
,则![]() 与
与![]() 的物质的量之比是 ______ ,这种混合气体的密度是同温同压下氧气密度的 ______ 倍
的物质的量之比是 ______ ,这种混合气体的密度是同温同压下氧气密度的 ______ 倍![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物实际存在且命名正确的是 ( )
A. 3-甲基-2-丁烯 B. 2-甲基-5-乙基-1-已烷
C. 2,2-二甲基丁烷 D. 3,3-二甲基-2-戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及硫化物广泛存在于自然界中,回答下列问题:
(1)基态S原子中,核外电子占据的最高能层的符号是___________,有__________种不同形状的电子云。
(2)(NH4)2SO4中O、N、S三种元素的第一电离能的大小关系为_______________________。
(3)中学化学常用KSCN检验Fe3+,列举一种与SCN-互为等电子体的分子:___________,SCN-中C原子的杂化方式为_________________。
(4)乙硫醇(CH3CH2SH)的相对分子质量比CH3CH2OH大,但乙醇的沸点高于乙硫醇的原因是_________________________________________________。
(5)PbS是一种重要的半导体材料,具有NaC1型结构(如图),其中阴离子采用面心立方最密堆积方式,X-射线衍射实验测得PbS的晶胞参数为a=0.594 n m。

①已知坐标参数:A(0,0,0),B![]() ,则C的坐标参数为__________________。
,则C的坐标参数为__________________。
②PbS晶体中Pb2+的配位数为_________,r(S2-)为______nm。(已知![]() )
)
③PbS晶体的密度为_________g·cm-3。(列出计算式即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com