
【题目】根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是

A. 甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙
B. 生成1mol H2O时吸收热量245kJ
C. H2O分解为H2与O2时放出热量
D. 氢气和氧气的总能量小于水的能量
【答案】A
【解析】
上图表示了1mol氢气和0.5mol氧气反应生成1mol水的过程中的能量变化,断键吸收能量,成键释放能量,△H=反应物键能和-生成物键能和,据此解答。
A.断键吸收能量,成键释放能量,甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙,故A正确;
B.上述反应△H=反应物键能和-生成物键能和=436kJ/mol+249kJ/mol-930kJ/mol=-245kJ/mol,反应放热,所以水分解吸热,但是上述反应没有标注物质状态,具体放出多少热量无法确定,故B错误;
C. 据B分析,水分解吸热,故C错误;
D. 反应放热,反应物总能量高于生成物,氢气和氧气的总能量大于水的能量,故D错误;
答案选A。


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】已知HCN、CN-在溶液中存在下列平衡及其对应的平衡常数:①HCN![]() H++ CN- △H 1>0,K1 ②CN-+H2O
H++ CN- △H 1>0,K1 ②CN-+H2O ![]() HCN+OH- △H 2>0,K2,常温下(K1= 6.2×10-10),将等体积、等物质的量浓度的HCN和NaCN溶液混合,下列叙述正确的是( )
HCN+OH- △H 2>0,K2,常温下(K1= 6.2×10-10),将等体积、等物质的量浓度的HCN和NaCN溶液混合,下列叙述正确的是( )
A. 混合溶液的pH<7
B. 对混合溶液进行微热,K1 增大、K2 减小
C. K2≈ 1.6×10-5
D. c(Na+) = c(HCN) + c(CN—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)该学生的实验操作如下:
A.用碱式滴定管取待测NaOH溶液25.00mL,注入锥形瓶中,加入2滴酚酞;
B.用待测定的溶液润洗碱式滴定管
C.用蒸馏水洗干净滴定管
D.取下酸式滴定管用标准液的润洗后,将标准液注入酸式滴定管刻度“0”以上2-3cm处,再把酸式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作2次
G.把锥形瓶放在滴定管下面,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
滴定操作的正确顺序是___________
(2)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_________________,直到因加入一滴盐酸后,溶液由________变为________,即到达滴定终点。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是__________
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(4)若滴定开始和结束时,酸式滴定管中的液面如下图所示,则所用盐酸溶液的体积为________mL。

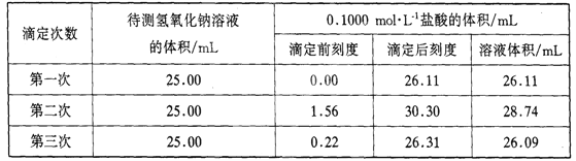
(5)某学生根据三次实验分别记录有关数据如下:请选用其中合理的数据计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO(g) + 2H2(g) ![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ: CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1____0 (填“>”、“=”或“<”)。
② 某温度下,将2mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为___________,此时的温度为_______(从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH1=-1451.6kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2 =-566.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_________________________________________
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:

①该电池的能量转化形式为___________________________。
②工作一段时间后,测得溶液的pH减小。请写出该电池的负极的电极反应式。_____________________________
③用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为___________mol/L(假设电解前后溶液体积不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
B. 相同温度时,1mol/L氨水与0.5mol/L氨水中,c(OH-)之比是2∶1
C. 已知2SO2(g)+ O2(g)![]() 2SO3 (g)△H<0,该反应在任何温度下均可自发进行
2SO3 (g)△H<0,该反应在任何温度下均可自发进行
D. 室温下,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=9.0×10-12,向浓度相等的Na2CrO4和NaCl的混合稀溶液中滴加0.01 mol·L-1 AgNO3溶液,先生成Ag2CrO4沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组用镍触媒废料(主要成分为Ni-Al合金,混有少量Fe、Cu、Zn及有机物) 制备NiO并回收金属资源的流程如下所示:

已知:相关数据如表1和表2所示
表1部分难溶电解质的溶度积常数(25℃)
物质 | Ksp | 物质 | Ksp |
Fe(OH)3 | 4.0×10-38 | CuS | 6.3×10-34 |
Fe(OH)2 | 1.8×10-16 | ZnS | 1.6×10-24 |
Al(OH)3 | 1.0×10-33 | NiS | 3.2×10-18 |
Ni(OH)2 | 2.0×10-15 |
表2 原料价格表
物质 | 价格/(元吨-1) |
漂液(含25.2%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
请回答下列问题:
(1)“焙烧”的目的是________________________________。
(2)“试剂a”的名称为__________________;选择该试剂的理由是______。
(3)“氧化”时反应的离子方程式为__________________________________________。
(4)欲使溶液中Fe3+和A13+的浓度均小于等于1.0×10-6 mol L-1,需“调节pH”至少为_______________。
(5)“试剂b”应选择__________,“加水煮沸”时,反应的化学方程式为_______________________________。
(6)氢镍电池是一种应用广泛的二次电池,放电时,该电池的总反应为NiOOH+MH=Ni(OH)2+M,当导线中流过2 mol电子时,理论上负极质量减少__________g。充电时的阳极反应式为_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,△H1=-393.5 kJmol-1,△H2=-395.4 kJmol-1,下列说法或表示式正确的是( )

A. C(s、石墨)==C(s、金刚石)△H=+1.9kJmol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列五种物质A.食盐, B.食醋,C.苹果汁,D.葡萄糖,E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是____;可直接进入血液,补充能量的是___ ;应用最广泛的抗生素之一的是____;即可作为调味剂,又可作为防腐剂、着色剂的是____;食用过多会引起血压升高、肾脏受损的____。
(2)已知维生素A1的键线式如下,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。

回答下列问题:
①维生素A是一类重要的维生素,又称视黄醇,它属于_____(填“水溶性”或“脂溶性”)维生素;如果人体内缺少维生素A,易患_____等眼疾(任写一种), 维生素A含量较高的蔬菜有______。
②维生素A1的结构简式如上图,推测它____使溴水褪色(填“能”或“否”),若1mol维生素A1分子最多可跟_____mol H2发生加成反应。
(3)保持洁净安全的生存环境已成为全人类的共识。
①为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行______。对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为______。
②获得洁净安全的饮用水是每个人的正常需要。某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉或漂白精片进行杀菌消毒,其原理可用化学方程式表示为_______。
③人类产生的垃圾应进行分类回收、集中处理,即便如此,仍会剩余不少垃圾,因此必须对剩余垃圾进一步处理,除卫生填埋外,还有一种能够改变垃圾的组成、结构使其体积减小、充分利用其所具有的能量并使之无害化的处理方式,这种垃圾的处理方式是_____技术。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲基丙烯酸甲酯是世界上年产量超过100万吨的高分子单体,旧法合成的反应是
(CH3)2C==O+HCN→ (CH3)2C(OH)CN
(CH3)2C(OH)CN+CH3OH+H2SO4→CH2== C(CH3)COOCH3+NH4HSO4,
90年代新的反应是:CH3C≡CH+CO+CH3OH![]() CH2==C(CH3)COOCH3,与旧法比较,新法的优点是:①原料无爆炸危险 ;②原料都是无毒物质;③没有副产物,原料利用率高;④对设备腐蚀性较小。正确的是
CH2==C(CH3)COOCH3,与旧法比较,新法的优点是:①原料无爆炸危险 ;②原料都是无毒物质;③没有副产物,原料利用率高;④对设备腐蚀性较小。正确的是
A. ①② B. ③④ C. ①③ D. ②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com