
| A. | ④②①③ | B. | ①③②④ | C. | ③②④① | D. | ③④①② |
分析 葡萄糖含有醛基,可与新制Cu(OH)2发生氧化还原反应;淀粉遇碘变蓝色;AgNO3溶液与含氯离子的物质反应生成白色的沉淀;浓硝酸能使蛋白质呈现黄色,以此来解答.
解答 解:葡萄糖的结构简式为CH2OH(CHOH)4CHO,含有醛基,含有醛基的物质与新制Cu(OH)2悬浊液反应生成砖红色沉淀,可用新制Cu(OH)2发检验葡萄糖;
淀粉溶液与碘水作用显示蓝色,可用碘水检验淀粉;
食盐为氯化钠,在溶液中电离出氯离子,与硝酸银电离出银离子结合,生成白色的氯化银沉淀,可用硝酸银检验食盐溶液;
鸡蛋清是蛋白质,蛋白质遇浓硝酸发生显色反应,可用硝酸检验蛋白质,
则加入上述试剂的正确顺序是③④①②,
故选D.
点评 本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同为解答该题的关键,题目难度不大.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:实验题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
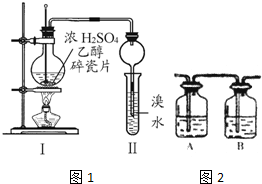 某化学兴趣小组用如图所示装置进行探究性实验,验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变成棕黑色(棕黑色是浓硫酸将无水乙醇氧化生成碳单质等多种物质,碳单质使烧瓶内的液体带上了黑色)
某化学兴趣小组用如图所示装置进行探究性实验,验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变成棕黑色(棕黑色是浓硫酸将无水乙醇氧化生成碳单质等多种物质,碳单质使烧瓶内的液体带上了黑色) .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
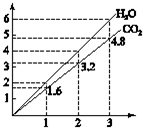 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )| A. | ②⑤⑥ | B. | ④⑥ | C. | ①②④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
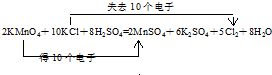 .
.
 ,氯原子核外有17不同运动状态的电子.
,氯原子核外有17不同运动状态的电子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O | |
| B. | CH3CH2OH+HBr$\stackrel{△}{→}$C2H5Br+H2O | |
| C. | 2CH3CH2OH$→_{140℃}^{浓硫酸}$C2H5OC2H5+H2O | |
| D. | CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com